题目内容
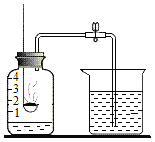
【题目】已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:
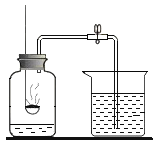
(1)红磷在集气瓶中发生反应的现象:_____;该实验中红磷需稍过量,其目的是:_____;
(2)若未冷却到室温就打开止水夹,会导致测出的氧气含量偏_____(填“高”或“低”);
(3)已知:3Mg+N2![]() Mg3N2(固体),2Mg+CO2
Mg3N2(固体),2Mg+CO2![]() 2MgO+C.根据上述反应可知,能否用镁代替红磷测定空气中氧气的含量?_____,为什么?_____.
2MgO+C.根据上述反应可知,能否用镁代替红磷测定空气中氧气的含量?_____,为什么?_____.
【答案】产生大量白烟,放热 保证瓶内氧气完全消耗 低 不能 因为镁在空气中燃烧时,与氧气、二氧化碳和氮气都能够发生反应, 这样进入集气瓶内水的体积必然大于氧气的体积
【解析】
(1)红磷在集气瓶中发生反应时能够产生大量白烟,放出大量的热; 该实验中红磷需稍过量,其目的是使容器中的氧气完全反应.
故填:产生大量白烟,放热;保证瓶内氧气完全消耗.
(2)若未冷却到室温就打开止水夹,由于集气瓶中的温度很高,气体压强较大, 会导致进入集气瓶中的水偏少,从而会导致测出的氧气含量偏低.
故填:低.
(3)不能用镁代替红磷测定空气中氧气的含量,这是因为镁在空气中燃烧时,与氧气、二氧化碳和氮气都能够发生反应,这样进入集气瓶内水的体积必然大于氧气的体积,会导致测定的氧气含量偏高.
故填:不能;因为镁在空气中燃烧时,与氧气、二氧化碳和氮气都能够发生反应, 这样进入集气瓶内水的体积必然大于氧气的体积.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目