题目内容
某校化学兴趣小组的同学利用下列装置进行实验.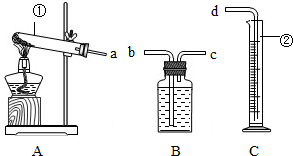
实验目的:(1)用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验.
(2)粗略测定加热2g高锰酸钾所收集到的氧气体积.
反应原理:(用化学方程式表示)
高锰酸钾制氧气:
细铁丝在氧气中燃烧:
仪器认识:写出仪器①②的名称:①
装置连接:为达到实验目的(2),各装置的正确连接顺序是:(填接口的字母)a→
问题分析:(1)实验过程发现B瓶中的水变红了,原因是:
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能是:
(3)根据化学方程式可算出理论上2g高锰酸钾完全分解可生成氧气0.203g.而实际测得氧气在标准状况下的体积为177mL,换算成质量为0.253g,超过理论量为:0.253g一0.203g=0.05g.从理论上推测,你认为超过理论量的氧气可能来源于什么物质?
分析:反应原理:①高锰酸钾制氧气:知其反应物为高锰酸钾,生成物为锰酸钾、二氧化锰、氧气,反应条件为加热,可书写化学方程式;②细铁丝在氧气中燃烧:知其反应物为铁和氧气,生成物为四氧化三铁,反应条件为点燃,可书写出化学方程式;
仪器认识:了解常用仪器的名称和应用,即可轻松解答;
装置连接:为达到实验目的粗略测定加热2g高锰酸钾所收集到的氧气体积,则各装置的正确连接顺序是a→c→b→d;
问题分析:由图知:(1)装置A试管口缺少一团棉花,会导致KMnO4冲入导管,进入B瓶,使水变红;
(2)铁丝燃烧实验集气瓶应保留少量水,以免细铁丝在氧气中燃烧,瓶底炸裂;
(3)中水的体积即为收集的氧气的体积.制得氧气的实际量高于理论量,题中提示除去可能混有空气、水因素外,只可能来源于含有氧元素的生成物K2MnO4、MnO2.
仪器认识:了解常用仪器的名称和应用,即可轻松解答;
装置连接:为达到实验目的粗略测定加热2g高锰酸钾所收集到的氧气体积,则各装置的正确连接顺序是a→c→b→d;
问题分析:由图知:(1)装置A试管口缺少一团棉花,会导致KMnO4冲入导管,进入B瓶,使水变红;
(2)铁丝燃烧实验集气瓶应保留少量水,以免细铁丝在氧气中燃烧,瓶底炸裂;
(3)中水的体积即为收集的氧气的体积.制得氧气的实际量高于理论量,题中提示除去可能混有空气、水因素外,只可能来源于含有氧元素的生成物K2MnO4、MnO2.
解答:解:反应原理:依据反应物、生成物及质量守恒定律书写方程式如下:2KMnO4
K2MnO4+MnO2+O2↑;3Fe+2O2
Fe3O4;
仪器认识:了解常用仪器的名称和应用,可知①试管,②量筒;
装置连接:为达到实验目的粗略测定加热2g高锰酸钾所收集到的氧气体积,首先用A装置制取氧气,B装置收集气体,为了便于水的排出用来测量生成氧气体积,从c进d出,各装置的正确连接顺序是a→c→b→d;
问题分析:(1)用高锰酸钾制取一瓶氧气,试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管,进而进入瓶中,因此,实验过程中发现B瓶中水变红了,原因是试管口没有放一团棉花或高锰酸钾粉末进入瓶中;
(2)用收集到的氧气做细铁丝燃烧的实验时,瓶底要预先放一些水,防止燃烧后的熔融物溅落瓶底,引起瓶底炸裂;
(3)C中水的体积即为收集的氧气的体积,制得氧气的实际量高于理论量,超出的氧气不会凭空产生,因为题中提示除去可能混有空气、水因素外,依据质量守恒定律化学反应前后元素的种类不变,只可能来源于含有氧元素的是K2MnO4、MnO2.
故答案为:
2KMnO4
K2MnO4+MnO2+O2↑;3Fe+2O2
Fe3O4;
①试管②量筒;c、b;
(1)试管口没有放一团棉花或高锰酸钾粉末进入瓶中;
(2)瓶中没有留少量水;
(3)K2MnO4、MnO2
| ||
| ||
仪器认识:了解常用仪器的名称和应用,可知①试管,②量筒;
装置连接:为达到实验目的粗略测定加热2g高锰酸钾所收集到的氧气体积,首先用A装置制取氧气,B装置收集气体,为了便于水的排出用来测量生成氧气体积,从c进d出,各装置的正确连接顺序是a→c→b→d;
问题分析:(1)用高锰酸钾制取一瓶氧气,试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管,进而进入瓶中,因此,实验过程中发现B瓶中水变红了,原因是试管口没有放一团棉花或高锰酸钾粉末进入瓶中;
(2)用收集到的氧气做细铁丝燃烧的实验时,瓶底要预先放一些水,防止燃烧后的熔融物溅落瓶底,引起瓶底炸裂;
(3)C中水的体积即为收集的氧气的体积,制得氧气的实际量高于理论量,超出的氧气不会凭空产生,因为题中提示除去可能混有空气、水因素外,依据质量守恒定律化学反应前后元素的种类不变,只可能来源于含有氧元素的是K2MnO4、MnO2.
故答案为:
2KMnO4
| ||
| ||
①试管②量筒;c、b;
(1)试管口没有放一团棉花或高锰酸钾粉末进入瓶中;
(2)瓶中没有留少量水;
(3)K2MnO4、MnO2
点评:本题切入点新颖,结合氧气的制取和定量收集设计,解题时要注意结合自己的实践经验和亲身体验,根据观察到的现象和记录的数据进行推理和判断.

练习册系列答案
相关题目
某校化学兴趣小组的同学经查阅资料知道:淀粉在适当温度和酸催化条件下可转变为葡萄糖.为探究淀粉在不同温度下转化为葡萄糖的程度,他们每人都进行了如下两步实验:
步骤1.用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度.实验过程中,各人控制温度不同,加热持续时间相同.
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水.观察并记录现象.
(1)由于各人控制的温度不同,出现了下列三种情况.请你根据已学知识,帮助他们完成下列实验情况汇总表.
(2)在步骤2中A试管内所加Na0H溶液的作用是 .
步骤1.用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度.实验过程中,各人控制温度不同,加热持续时间相同.
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水.观察并记录现象.
(1)由于各人控制的温度不同,出现了下列三种情况.请你根据已学知识,帮助他们完成下列实验情况汇总表.
| 现 象 | 结 论 | |
| 第一种 情 况 | A试管中: B试管中: | 淀粉没有转化为葡萄糖 |
| 第二种 情 况 | A试管中: B试管中: | |
| 第三种 情 况 | A试管中: B试管中: | 淀粉全部转化为葡萄糖 |
某校化学兴趣小组的同学经查阅资料知道:淀粉在适当温度和酸催化条件下可转变为葡萄糖.为探究淀粉在不同温度下转化为葡萄糖的程度,他们每人都进行了如下两步实验:
步骤1.用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度.实验过程中,各人控制温度不同,加热持续时间相同.
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水.观察并记录现象.
(1)由于各人控制的温度不同,出现了下列三种情况.请你根据已学知识,帮助他们完成下列实验情况汇总表.
(2)在步骤2中A试管内所加Na0H溶液的作用是 .
步骤1.用一支大试管取一定量淀粉与水混合,再加入适量的稀硫酸,摇匀,加热到一定的温度.实验过程中,各人控制温度不同,加热持续时间相同.
步骤2.然后用两支小试管各取少量大试管内的反应混合物,在其中一支小试管(编号为A)内滴加NaOH溶液至呈强碱性,再滴入4-5滴CuS04溶液,并加热至沸;在另一支小试管(编号为B)内滴加2-3滴碘水.观察并记录现象.
(1)由于各人控制的温度不同,出现了下列三种情况.请你根据已学知识,帮助他们完成下列实验情况汇总表.
| 现 象 | 结 论 | |
| 第一种 情 况 | A试管中: B试管中: | 淀粉没有转化为葡萄糖 |
| 第二种 情 况 | A试管中: B试管中: | |
| 第三种 情 况 | A试管中: B试管中: | 淀粉全部转化为葡萄糖 |
