题目内容
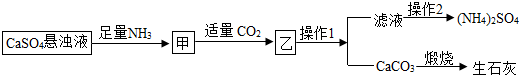
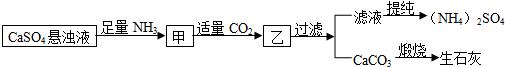
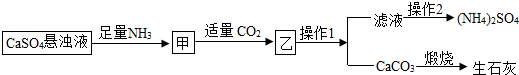
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
下列推断不合理的是( )
A.操作1、操作2均为过滤
B.整个流程的总反应的方程式为:CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓
C.该流程中CO2可被循环使用
D.此过程中若先通CO2 后通NH3能提高生产效率
【答案】分析:A、依据过滤能够分离的混合物种类分析解答;
B、依据整个过程的反应物以及生成物情况分析解答;
C、依据碳酸钙高温分解产生的二氧化碳可以在第二步循环利用;
D、依据氨气和二氧化碳反应生成碳酸铵,然后碳酸铵和硫酸钙反应得到硫酸铵和碳酸钙.
解答:解:A、操作1是不溶性固体与液体的分离应是过滤;操作2是可溶性固体与液体的分离应是蒸发;故错.
B、依据对整个过程的分析以及制取硫酸铵的目的分析可知:整个流程的总反应的方程式为:CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓煅烧碳酸钙生成氧化钙和二氧化碳,生成的二氧化碳可以循环使用;故对.
C、煅烧碳酸钙生成氧化钙和二氧化碳,生成的二氧化碳可以循环使用;故对.
D、先通入氨气使溶液呈碱性,这样能增加二氧化碳的溶解量,从而能提高生产效率,故错.
故选AD.
点评:解答本题时要充分理解图中提供的信息,只有理解了图中信息才能对问题做出正确的判断.
B、依据整个过程的反应物以及生成物情况分析解答;
C、依据碳酸钙高温分解产生的二氧化碳可以在第二步循环利用;
D、依据氨气和二氧化碳反应生成碳酸铵,然后碳酸铵和硫酸钙反应得到硫酸铵和碳酸钙.
解答:解:A、操作1是不溶性固体与液体的分离应是过滤;操作2是可溶性固体与液体的分离应是蒸发;故错.
B、依据对整个过程的分析以及制取硫酸铵的目的分析可知:整个流程的总反应的方程式为:CaSO4+2NH3+CO2+H2O=(NH4)2SO4+CaCO3↓煅烧碳酸钙生成氧化钙和二氧化碳,生成的二氧化碳可以循环使用;故对.
C、煅烧碳酸钙生成氧化钙和二氧化碳,生成的二氧化碳可以循环使用;故对.
D、先通入氨气使溶液呈碱性,这样能增加二氧化碳的溶解量,从而能提高生产效率,故错.
故选AD.
点评:解答本题时要充分理解图中提供的信息,只有理解了图中信息才能对问题做出正确的判断.

练习册系列答案
相关题目