题目内容
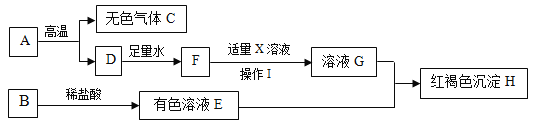
【题目】知识网络图有助于知识间的融合。下图是初中化学部分常见物质之间的转化关系,其中A是一种建筑材料的主要成分,B属于金属氧化物,X的俗名叫苏打。请回答:
(1)写出下列物质的化学式:A._____, X。_____。
(2)化学反应常伴有能量变化。D与水反应时会_____(“吸收”或“放出”)热量。
(3)由F与X反应后得到G溶液的实验操作Ⅰ名称是_____。
(4)写出B+稀盐酸→E的反应化学方程式为_____。
【答案】![]()
![]() 放出 过滤
放出 过滤 ![]()
【解析】
A是建筑材料的主要成分,A在高温下又会生成无色气体C和D,A是碳酸钙,C是二氧化碳,D是氧化钙,F是氢氧化钙,X的俗名叫苏打,X是碳酸钠,F和X生成G,G是氢氧化钠,H是红褐色沉淀,H是氢氧化铁,B属于金属氧化物,E是氧化物B和盐酸反应产生的氯化铁,B是氧化铁,E是氯化铁。
(1)A是建筑材料的主要成分,A在高温下又会生成无色气体C和D,A是碳酸钙,X的俗名叫苏打,X是碳酸钠,故物质的化学式:A是![]() ,X是
,X是![]() 。
。
(2)D是氧化钙,氧化钙和水反应生成氢氧化钙,D与水反应时会放出热量。
(3)F与X反应是氢氧化钙和碳酸钠生成碳酸钙和氢氧化钠,由F与X反应后得到G溶液的实验操作Ⅰ名称是过滤。
(4)B+稀盐酸→E的反应是盐酸和氧化铁反应生成氯化铁和水,反应化学方程式为![]() 。
。

 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】硝酸(HNO3)是实验室常见的一种酸。实验小组对硝酸的某些性质进行研究。
Ⅰ、挥发性
(实验1)取一瓶质量分数为68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到_____,原因是_____。
Ⅱ、不稳定性
(查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体、氧气及一种无色液体
(1)硝酸分解的化学方程式为:_____。
(实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26℃)。记录溶液上方的气体颜色随时间的变化情况。
实验编号 | ① | ② | ③ |
实验条件 |
|
|
|
实验现象 | 6分钟出现浅红棕色 15分钟红棕色比较明显 30分钟红棕色非常明显 | 60分钟无明显变化 | 3分钟出现浅红棕色 6分钟红棕色比较明显 10分钟红棕色非常明显 |
(2)实验①、②对比是研究_____对浓硝酸稳定性的影响。
(3)实验①、③对比可得出的结论是_____。
Ⅲ、酸性
(查阅资料2)硝酸能够与金属氧化物反应生成盐和水。
(实验3)向氧化铜粉末中加入硝酸,能够看到的现象是_____。
IV、氧化性
(查阅资料3)浓硝酸在加热条件下能与木炭发生反应:
C+4HNO3(浓)![]() 4NO2↑+CO2↑+2H2O。
4NO2↑+CO2↑+2H2O。
(实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能是_____。

【题目】某化学兴趣小组发现了一包敞口放置的碱石灰样品,为探究其成分,同学们在实验室对这包碱石灰样品展开了探究。
[查阅资料]①碱石灰是由CaO和NaOH固体混合而成,通常用于吸收二氧化碳及干燥气体。
②熟石灰微溶于水,且溶于水放出的热量很少可以忽略不计。
③CaC12溶液显中性。
(1)[提出猜想]根据资料,同学们分析该碱石灰样品的主要成分可能含有CaO、NaOH、Na2CO3、CaCO3和_____。
(2)[实验探究]小组同学讨论后设计如下实验进行探究:
实验步骤及操作 | 实验现象 | 结论 |
①取部分该样品于试管中,加少量水 | 无明显放热现象 | 石灰样品中不含CaO和_____ |
②继续加足量水,震荡,静置 | 出现白色沉淀 | 样品中一定含有CaCO3 |
③从步骤②的试管中取少量上层清液于另一试管中,向其中滴加过量CaCl2溶液 | 产生白色沉淀 | |
④将步骤③所得物质过滤,向滤液中滴加无色酚酞试液 | 溶液变红色 |
(3)[思考与分析]小宇同学经过分析认为步骤②的结论不正确,原因是_____(用化学方程式表示)。
(4)[解释与结论]通过以上探究与分析可以得出碱石灰样品一定含有的物质是_____;可能含有的物质是_____。实验探究步骤④所得溶液中除酚酞外,还含有的溶质有_____。