题目内容
碳与碳的化合物在工农业生产及日常生活中有广泛的用途.(1)图是碳原子结构示意图,碳原子的最外层电子数是
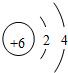
(2)古代用墨书写或绘制的字画虽年久仍不变色,原因是墨中主要成分碳在常温下具有
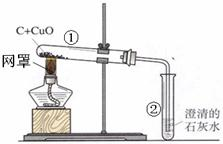
③继续加热,观察到石灰水逐渐变浑浊,黑色粉末中出现红色物质.请你写出带点部分的化学方程式:
④停止加热时,应先将导管从试管②中撤出,待试管①冷却后再把试管里的粉末倒出.这样操作的原因是
A
B
(3)二氧化碳能参与光合作用完成大气中的“碳循环”,但是大气中二氧化碳的含量不断上升,会使全球变暖,从而导致
(4)研究发现:物质的结构决定性质,物质的性质决定用途.如:一氧化碳也能还原氧化铜,也有还原性.从化学反应前后碳元素化合价的变化特点分析,一氧化碳和碳都具有还原性的原因是
分析:根据原子的结构示意图可以判断原子的最外层电子数,电子层数表示该元素所处的周期;常温下碳的化学性质不活泼,我国古代用墨书写、绘制的字画,可以多年保存而不褪色,埋在地下的电线杆烧焦等,就是利用碳单质在常温下的稳定性.碳有较强的还原性,能夺取金属氧化物如CuO、Fe2O3、Fe3O4等中的氧生成金属和使澄清的石灰水变浑浊的气体二氧化碳,常用于冶金工业.二氧化碳是温室气体之一,有利有弊,还能做为气体肥料用在农业中;由同类元素组成的一氧化碳却有毒性,而且也跟碳单质一样具有还原性,其根本原因就是碳单质和一氧化碳中碳元素的化合价都为中间价态,都能够夺取金属氧化物中的氧而变为+4价的碳.
解答:解:(1)由碳原子的结构示意图可知,碳原子的最外层电子数4,因为电子层数就表示该元素所处的周期,所以碳元素位于第二周期,故答案为:4,二.
(2)常温下碳的化学性质不活泼,我国古代用墨书写、绘制的字画,可以多年保存而不褪色,就是利用碳单质在常温下的稳定性.碳另一个化学性质就是有较强的还原性,能夺取金属氧化物如CuO、Fe2O3、Fe3O4等中的氧生成金属和使澄清的石灰水变浑浊的气体二氧化碳,由于反应须在高温条件下进行,因此实验过程中,酒精灯加灯罩,其目的就是使火焰集中,提高温度.实验开始,反应不能立即进行,试管中的空气受热膨胀排出,故开始时排出的气体不能使澄清的石灰水变浑浊,随着反应的进行,碳与氧化铜在高温下反应,生成二氧化碳,化学方程式为:C+2CuO
2Cu+CO2,Ca(OH)2+CO2=CaCO3↓+H2O;实验结束时应先将导管从石灰水中取出,防止溶液倒吸炸裂试管,然后冷却后再将大试管中的粉末倒出,防止还原生成的铜被空气中的氧气重新氧化.
以本题答案:稳定性;①使火焰集中并提高温度;②开始排出的气体是空气;
③Ca(OH)2+CO2=CaCO3↓+H2O;④防止石灰水倒流导致试管①破裂;防止生成的铜被氧化.
(3)二氧化碳是温室气体之一,大量排放导致温室效应,但二氧化碳还能做为气体肥料用在农业中,
所以本题答案为:温室效应;H2SO4+2NH4HCO3=(NH4)2SO4+2H2O+2CO2↑.
(4)碳单质中,碳元素的化合价为0价,一氧化碳中碳元素的化合价为+2价,在二氧化碳中碳元素的化合价为+4价,
所以本题答案为:碳元素的化合价小于+4.
(2)常温下碳的化学性质不活泼,我国古代用墨书写、绘制的字画,可以多年保存而不褪色,就是利用碳单质在常温下的稳定性.碳另一个化学性质就是有较强的还原性,能夺取金属氧化物如CuO、Fe2O3、Fe3O4等中的氧生成金属和使澄清的石灰水变浑浊的气体二氧化碳,由于反应须在高温条件下进行,因此实验过程中,酒精灯加灯罩,其目的就是使火焰集中,提高温度.实验开始,反应不能立即进行,试管中的空气受热膨胀排出,故开始时排出的气体不能使澄清的石灰水变浑浊,随着反应的进行,碳与氧化铜在高温下反应,生成二氧化碳,化学方程式为:C+2CuO
| ||
以本题答案:稳定性;①使火焰集中并提高温度;②开始排出的气体是空气;
③Ca(OH)2+CO2=CaCO3↓+H2O;④防止石灰水倒流导致试管①破裂;防止生成的铜被氧化.
(3)二氧化碳是温室气体之一,大量排放导致温室效应,但二氧化碳还能做为气体肥料用在农业中,
所以本题答案为:温室效应;H2SO4+2NH4HCO3=(NH4)2SO4+2H2O+2CO2↑.
(4)碳单质中,碳元素的化合价为0价,一氧化碳中碳元素的化合价为+2价,在二氧化碳中碳元素的化合价为+4价,
所以本题答案为:碳元素的化合价小于+4.
点评:本题综合考查碳和碳的化合物的有关性质,碳单质的可燃性和还原性是碳的重要化学性质,而碳单质跟氧化铜和二氧化碳的反应则是难点,要解答此情境题必须对碳单质的化学性质:(1)稳定性;(2)可燃性;(3)还原性及其化学反应原理有比较深的理解,综合性较强.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
 17、碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
17、碳与碳的化合物在工农业生产及日常生活中有广泛的用途.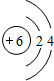 碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
碳与碳的化合物在工农业生产及日常生活中有广泛的用途.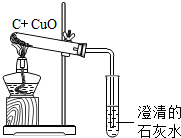 (3)二氧化碳能参与光合作用完成大气中的“碳循环”,但是
(3)二氧化碳能参与光合作用完成大气中的“碳循环”,但是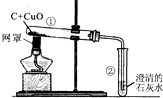 碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
碳与碳的化合物在工农业生产及日常生活中有广泛的用途.