题目内容
小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应。实验完毕后,称得所得固体的质量小于4.0g。
【提出问题】固体质量为什么会小于4.0g呢?是否发生了其他 反应呢?
反应呢?
【查阅资料】镁在空气中燃烧时,除了镁与氧气反应外,还可发生反应:
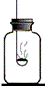 ①2Mg+CO2
①2Mg+CO2 C+2MgO ②3Mg+N2
C+2MgO ②3Mg+N2 Mg3N2
Mg3N2
【猜想与假设】反应后固体质量小于4.0g是由于发生反应 造成的。
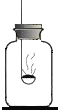
【实验探究】根据初中化学所学知识用图所示装置除去空气中的氧气得到氮气(含少量稀有气体).可燃物应选择的物质是 (填写物质的字母代号).
A.木炭 B.红磷 C.硫粉
选择的理由是 .
将点燃的镁条伸入所制得的氮气中,镁条在氮气中剧烈燃烧.
【实验结论】2.4g镁在空气中完全反应后所得固体质量小于4.0g,是由于生成的产物是氧化镁和氮化镁的混合物所致.
【评价与反思】通过上述实验,小林对燃烧有了新的认识: .
②、B、红磷只和氧气反应且不产生新的气体、燃烧不一定需要氧气(或氮气也能够支持燃烧 等)
等)

练习册系列答案
相关题目
 (2013?衡阳)小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为
(2013?衡阳)小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为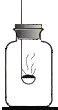 小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为________.实验完毕后,称得所得固体的质量小于4.0g.
小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为________.实验完毕后,称得所得固体的质量小于4.0g. C+2MgO ②3Mg+N2
C+2MgO ②3Mg+N2 C+2MgO ②3Mg+N2
C+2MgO ②3Mg+N2 Mg3N2
Mg3N2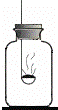
 反应呢?
反应呢?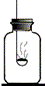 ①2Mg+CO2
①2Mg+CO2 C+2MgO ②3Mg+N2
C+2MgO ②3Mg+N2 Mg3N2
Mg3N2