题目内容
16、某学校的探究性学习小组发现,铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.他们通过实验探究,分析黑色固体的组成,并验证产生的气体.请填空:
(1)提出问题:黑色固体是什么?
(2)猜想与假设:黑色固体可能是:a.炭粉 b.氧化铜
(3)查阅资料:炭粉和氧化铜均为黑色固体,其中炭粉不与稀酸反应,也不溶于稀酸,而氧化铜可与稀酸反应而溶解.
(4)设计实验方案:
向试管中的黑色固体滴加足量的
(5)现象与结论:
如果猜想a正确,则现象为
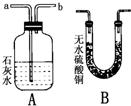
(6)若用如图装置验证两种气体生成物,应将生成的混合气体先通过
(7)交流与反思:
古代铜币表面绿色铜锈的主要成分是Cu2(OH)2CO3,文物鉴定人员常用酸验法鉴别铜锈真伪:
用细玻璃棒蘸取少许稀盐酸,涂擦在需要鉴别可疑铜锈的部位,若有气泡产生则初定为铜锈,反应的化学方程式为
(1)提出问题:黑色固体是什么?
(2)猜想与假设:黑色固体可能是:a.炭粉 b.氧化铜
(3)查阅资料:炭粉和氧化铜均为黑色固体,其中炭粉不与稀酸反应,也不溶于稀酸,而氧化铜可与稀酸反应而溶解.
(4)设计实验方案:
向试管中的黑色固体滴加足量的
H2SO4(或HCl)
(填化学式)溶液,充分反应后,观察固体的溶解情况和所得溶液的颜色.(5)现象与结论:
如果猜想a正确,则现象为
黑色固体不溶解,溶液呈无色
;若现象是
黑色固体完全溶解,溶液呈蓝色
,则猜想b正确.(6)若用如图装置验证两种气体生成物,应将生成的混合气体先通过
B
装置.
(7)交流与反思:
古代铜币表面绿色铜锈的主要成分是Cu2(OH)2CO3,文物鉴定人员常用酸验法鉴别铜锈真伪:
用细玻璃棒蘸取少许稀盐酸,涂擦在需要鉴别可疑铜锈的部位,若有气泡产生则初定为铜锈,反应的化学方程式为
Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑
.分析:(4)根据资料可知,通过黑色固体是否能与酸反应可判断黑色固体为炭粉还是氧化铜,因此可选择向黑色固体中滴加足量的酸观察反应后固体的溶解情况和所得溶液的颜色;
(5)由于黑色炭粉不能与酸发生反应,溶液无颜色变化;氧化铜能与酸生成可溶性铜盐而使溶液呈现蓝色.因此,根据反应后固体的溶解情况及溶液颜色对猜想进行判断;
(6)装置A用于检验生成气体中的二氧化碳,澄清石灰水变浑浊;装置B中无水硫酸铜遇水变成蓝色,可用于检验生成气体中的水蒸气;由于气体通过装置A后,会混有水,此时再把气体通过装置B则无法说明生成物中是否含水;
(7)根据离子间的共存关系判断铜锈与稀盐酸反应的生成物:碳酸根与H+形成水和二氧化碳,氢氧根与H+形成水,溶液中剩余铜离子和氯离子形成氯化铜溶液.
(5)由于黑色炭粉不能与酸发生反应,溶液无颜色变化;氧化铜能与酸生成可溶性铜盐而使溶液呈现蓝色.因此,根据反应后固体的溶解情况及溶液颜色对猜想进行判断;
(6)装置A用于检验生成气体中的二氧化碳,澄清石灰水变浑浊;装置B中无水硫酸铜遇水变成蓝色,可用于检验生成气体中的水蒸气;由于气体通过装置A后,会混有水,此时再把气体通过装置B则无法说明生成物中是否含水;
(7)根据离子间的共存关系判断铜锈与稀盐酸反应的生成物:碳酸根与H+形成水和二氧化碳,氢氧根与H+形成水,溶液中剩余铜离子和氯离子形成氯化铜溶液.
解答:解:(4)根据:炭粉不与稀酸反应,也不溶于稀酸,而氧化铜可与稀酸反应而溶解,可向黑色固体中滴加足量的稀硫酸或稀盐酸来检验黑色固体;
故答案为:H2SO4(或HCl);
(5)炭粉不与稀酸反应,也不溶于稀酸,因此,黑色固体若为黑色炭粉则会观察到:固体不溶解,溶液为无色;氧化铜可与稀酸反应而溶解,生成可溶性铜盐溶液呈蓝色,因此,黑色固体若为氧化铜则可观察到:固体溶解,溶液变成蓝色;
故答案为:黑色固体不溶解,溶液呈无色;黑色固体完全溶解,溶液呈蓝色;
(6)燃烧后的气体应先通过装置B检验生成物中的水,然后通过装置B检验生成气体中的二氧化碳;
故答案为:B;
(7)铜锈与稀盐酸反应,可生成氯化铜、水和二氧化碳气体放出;
故答案为:Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑.
故答案为:H2SO4(或HCl);
(5)炭粉不与稀酸反应,也不溶于稀酸,因此,黑色固体若为黑色炭粉则会观察到:固体不溶解,溶液为无色;氧化铜可与稀酸反应而溶解,生成可溶性铜盐溶液呈蓝色,因此,黑色固体若为氧化铜则可观察到:固体溶解,溶液变成蓝色;
故答案为:黑色固体不溶解,溶液呈无色;黑色固体完全溶解,溶液呈蓝色;
(6)燃烧后的气体应先通过装置B检验生成物中的水,然后通过装置B检验生成气体中的二氧化碳;
故答案为:B;
(7)铜锈与稀盐酸反应,可生成氯化铜、水和二氧化碳气体放出;
故答案为:Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑.
点评:无水硫酸为白色粉末,遇水会则变成蓝色,实验室常用其来检验水的存在;使用时一般连接在其它气体检验装置前,以避免检验其它气体的溶液对水检验的影响.

练习册系列答案
相关题目
 32、某学校的探究性学习小组发现,铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.他们通过实验探究,分析黑色固体的组成,并验证产生的气体.请填空:
32、某学校的探究性学习小组发现,铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.他们通过实验探究,分析黑色固体的组成,并验证产生的气体.请填空: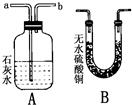 ,则猜想c成立.
,则猜想c成立.