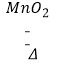题目内容
【题目】取氯酸钾和二氧化锰的混合物26g,加热至混合物固体质量不再减少为止,冷却后称得剩余固体质量为16.4g.计算:
(1)生成氧气的质量.
(2)二氧化锰的质量.
【答案】
(1)解:根据质量守恒定律,生成氧气的质量=26g﹣16.4g=9.6g
(2)解:设原混合物中氯酸钾的质量为x,
2KClO3 |
| 2KCl | 3O2↑ | |
245 | 96 | |||
x | 9.6g |
![]()
解得:x=24.5g
二氧化锰在该反应中充当了催化剂,其质量在反应前后不变,故二氧化锰的质量为:26g﹣24.5g=1.5g
【解析】(1)依据质量守恒定律反应前后固体的质量之差即为反应中生成的氧气质量;(2)利用氧气的质量结合方程式即可求出氯酸钾的质量,从而求出原反应混合物中含二氧化锰的质量分数.
【考点精析】解答此题的关键在于理解根据化学反应方程式的计算的相关知识,掌握各物质间质量比=系数×相对分子质量之比.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目