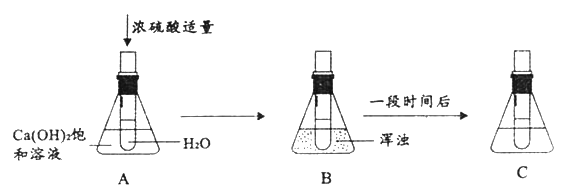
题目内容
【题目】请结合下列实验常用装置,回答有关问题。
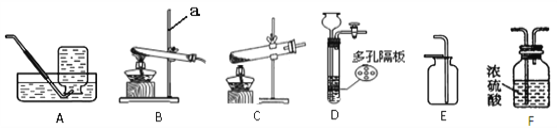
(1)写出仪器a的名称_____________。
(2)实验室用氯酸钾和二氧化锰制取氧气,可采用的发生装置为________,发生反应的化学方程式是_________________________________。
(3)实验室制取二氧化碳的化学方程式为_____________________________________,若要制取一瓶干燥的二氧化碳,可采用的装置组合为______________,若要使反应停止可采取的操作是_________________________________。
(4)为了证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳也能发生反应。如图所示进行实验(装置气密性良好,实验前活塞和弹簧夹K处于关闭状态)。
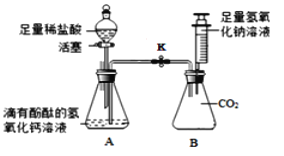
实验一:氢氧化钙溶液与稀盐酸发生反应打开分液漏斗的活塞,使稀盐酸逐滴滴加入A中锥形瓶,观察到______________的现象时,关闭活塞,证明氢氧化钙溶液与稀盐酸发生反应;
实验二:氢氧化钠与二氧化碳反应将注射器中的氢氧化钠溶液推入B中锥形瓶,过一段时间后,打开弹簧夹K,观察到_____________________的现象并且溶液呈红色,证明氢氧化钠溶液与二氧化碳确实发生了反应。请写出二氧化碳与氢氧化钠溶液反应的化学方程式是________________。锥形瓶B中溶液最后呈红色_________(填“能”或“不能”)证明氢氧化钠有剩余。
【答案】 铁架台 B 2KClO3 ![]() 2KCl+3O2↑ CaCO3+2HCl═CaCl2+H2O+CO2↑ DFE 关闭D中活塞,固液分离 溶液由红色变为无色 A瓶中液体进入B瓶中,且B瓶中出现白色沉淀(实验现象一定要写到白色沉淀才得分) Na2CO3+CaCl2=2NaCl+CaCO3↓ 不能
2KCl+3O2↑ CaCO3+2HCl═CaCl2+H2O+CO2↑ DFE 关闭D中活塞,固液分离 溶液由红色变为无色 A瓶中液体进入B瓶中,且B瓶中出现白色沉淀(实验现象一定要写到白色沉淀才得分) Na2CO3+CaCl2=2NaCl+CaCO3↓ 不能
【解析】(1)熟记常用仪器的名称可知a为铁架台;
(2)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置,固体加热时试管口应向下倾,C装置错误,故选B装置;氯酸钾以二氧化锰为催化剂加热生成氯化钾和氧气,化学方程式为:2KClO3 ![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳可以用浓硫酸干燥,因此应选择的装置组合是:DFE;若要使反应停止,关闭D中活塞,装置中气体无法排除,压强变大,液体被压回到长颈漏斗,固液分离,反应停止,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)开始时,氢氧化钙溶液显碱性,遇到酚酞显示红色,氢氧化钙与盐酸反应生成氯化钙和水,随着盐酸的滴入,烧杯中溶液红色逐渐褪去;当红色变为无色时,氢氧化钙溶液与稀盐酸发生反应;
将氢氧化钠溶液加入锥形瓶中,锥形瓶中的二氧化碳与氢氧化钠反应生成碳酸钠,压强变小,A装置中的压强大,打开弹簧夹K,就会将锥形瓶内的氯化钙流入B中,然后氯化钙与反应生成的碳酸钠反应,生成碳酸钙白色沉淀,因此有白色沉淀生成;化学方程式为:Na2CO3+CaCl2=2NaCl+CaCO3↓;由于碳酸钠溶液也显碱性,可以使酚酞变红,无法证明溶液最后呈红色,是否有氢氧化钠有剩余。