题目内容
【题目】空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:
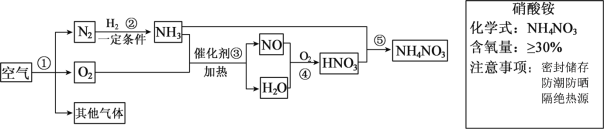
(1)空气中氮气的体积分数是__________。
(2)步骤①中发生的是________(填“物理”或“化学”)变化。
(3)写出步骤③中发生反应的化学方程式_____________。
(4)如图是化肥硝酸铵包装袋上的部分说明,硝酸铵应具有的性质是_________(填字母)。
A 易溶于水 B 熔点高 C 受热易分解
【答案】78% 物理 4NH3+5O2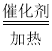 4NO+6H2O AC
4NO+6H2O AC
【解析】
(1)空气中氮气的体积分数为78%。
(2)步骤①中,利用空气中成分的沸点不同,可以把各种成分分离开来,过程中没有生成新物质,属于物理变化。
故填:物理。
(3)步骤③中,一定条件下氨气和氧气反应生成一氧化氮和水,发生反应的化学方程式为:4NH3+5O2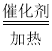 4NO+6H2O。
4NO+6H2O。
故填:4NH3+5O2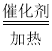 4NO+6H2O。
4NO+6H2O。
(4)硝酸铵应密封保存并且防潮,说明硝酸铵易溶于水,应该防晒隔热,说明硝酸铵受热易分解。
故填:AC。

【题目】某白色固体可能由BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种物质组成。某兴趣小组的同学为确定该白色固体的成分,进行了如下的实验探究,请你参与并回答。
Ⅰ.相关问题初步探究:小金同学设计的实验过程及现象如图所示:
(查阅资料)BaCl2溶液显中性。

(初步结论)
(1)原白色固体中一定有的物质是____,一定没有的物质是____。
(2)M溶液中的溶质一定没有_____。
(交流讨论)小英同学认为:无色溶液M变红色,说明溶液M中含有碱性物质,但不能由此推导出原固体物质中是否含有氢氧化钠。若要进一步确定,需对溶液M继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究
(提出问题)无色溶液M中有氢氧化钠吗?
(猜想与假设)猜想一:有NaOH; 猜想二:没有NaOH。
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
A.取无色溶液M于试管中,加入过量的氯化钡溶液,振荡,静置 | _______ | 证明溶液M中有碳酸钠并被除尽 |
B.取实验A所得上层清液于试管中,加入____。 | _________ | 猜想一正确 |