题目内容
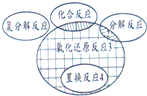
在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中错误的是( )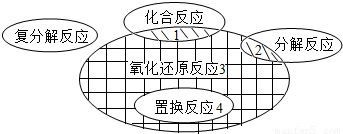
A.阴影1:C+O2
 CO2
CO2B.阴影2:2H2O
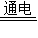 2H2↑+O2↑
2H2↑+O2↑C.阴影3:Mg(OH)2+2HCl=MgCl2+2H2O
D.阴影4:Fe+CuSO4=FeSO4+Cu
【答案】分析:复分解反应中各种元素化合价都没有升降,所以复分解反应都不是氧化还原反应.置换反应中元素化合价一定有升降,所以置换反应都是氧化还原反应.化合反应和分解反应中有的是氧化还原反应,有的不是氧化还原反应.
解答:解:A、C+O2 CO2中,碳氧两种元素的化合价都发生了变化,是氧化还原反应.
CO2中,碳氧两种元素的化合价都发生了变化,是氧化还原反应.
B、2H2O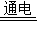 2H2↑+O2↑中,氢氧两种元素的化合价都发生了变化,是氧化还原反应.
2H2↑+O2↑中,氢氧两种元素的化合价都发生了变化,是氧化还原反应.
C、Mg(OH)2+2HCl═MgCl2+2H2O为复分解反应,各种元素的化合价都没有发生变化,不是氧化还原反应.
D、Fe+CuSO4=FeSO4+Cu中,铁铜两种元素的化合价都发生了变化,是氧化还原反应.
故选C.
点评:本题主要考查了氧化还原反应和其它反应类型的关系,可以依据已有的知识结合具体的反应进行.
解答:解:A、C+O2
 CO2中,碳氧两种元素的化合价都发生了变化,是氧化还原反应.
CO2中,碳氧两种元素的化合价都发生了变化,是氧化还原反应.B、2H2O
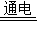 2H2↑+O2↑中,氢氧两种元素的化合价都发生了变化,是氧化还原反应.
2H2↑+O2↑中,氢氧两种元素的化合价都发生了变化,是氧化还原反应.C、Mg(OH)2+2HCl═MgCl2+2H2O为复分解反应,各种元素的化合价都没有发生变化,不是氧化还原反应.
D、Fe+CuSO4=FeSO4+Cu中,铁铜两种元素的化合价都发生了变化,是氧化还原反应.
故选C.
点评:本题主要考查了氧化还原反应和其它反应类型的关系,可以依据已有的知识结合具体的反应进行.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
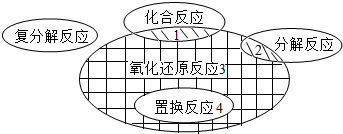 在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中错误的是( )
在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中错误的是( )A、阴影1:C+O2
| ||||
B、阴影2:2H2O
| ||||
| C、阴影3:Mg(OH)2+2HCl=MgCl2+2H2O | ||||
| D、阴影4:Fe+CuSO4=FeSO4+Cu |
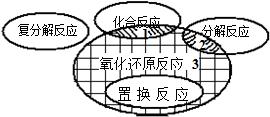
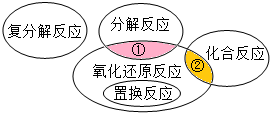 在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与九年级所学的化学基本反应类型间的关系如图所示.请各写出一例属于阴影①、②处的化学反应方程式
在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与九年级所学的化学基本反应类型间的关系如图所示.请各写出一例属于阴影①、②处的化学反应方程式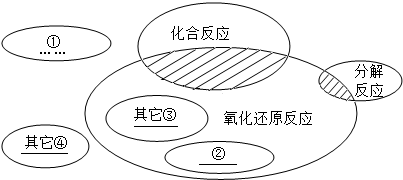
 在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中正确的是( )
在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中正确的是( )