题目内容
根据如图所示有关物质性质的实验,回答以下问题.
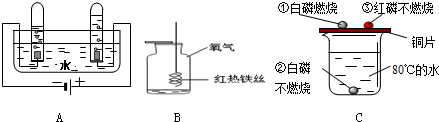
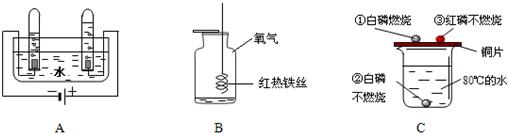
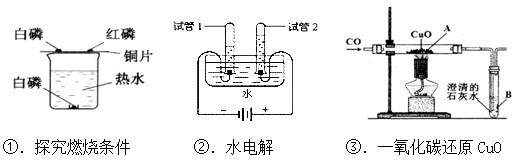
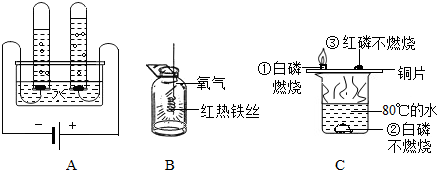
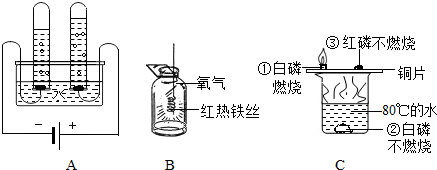
(1)装置A中,正极与负极产生气体分别是
(2)装置B中的现象:铁丝在氧气中剧烈燃烧,
(3)装置C中,由现象①说明铜能够

(1)装置A中,正极与负极产生气体分别是
氧气
氧气
和氢气
氢气
,体积比为1:2
1:2
.(2)装置B中的现象:铁丝在氧气中剧烈燃烧,
火星四射
火星四射
,放出大量的热,反应的化学方程式为3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
| ||
(3)装置C中,由现象①说明铜能够
导热
导热
;对比现象①②说明物质燃烧需要与氧气接触
与氧气接触
;对比现象①③说明两种可燃物的着火点
着火点
不同.分析:(1)该图表示的实验为电解水的实验,水通电时分解放出氢气和氧气,且两种气体的体积比为2:1;
(2)该项图表示的实验为铁丝在氧气中燃烧的实验,铁丝燃烧时,火星四射,生成黑色固体,放出大量热;
(3)该图所示的实验为燃烧条件的探究实验,放置于铜片上的白磷燃烧,而水中白磷、铜片上的红磷均不能燃烧,通过现象的对比与分析,可得出燃烧需要与氧气接触、温度达到可燃物的着火点.
(2)该项图表示的实验为铁丝在氧气中燃烧的实验,铁丝燃烧时,火星四射,生成黑色固体,放出大量热;
(3)该图所示的实验为燃烧条件的探究实验,放置于铜片上的白磷燃烧,而水中白磷、铜片上的红磷均不能燃烧,通过现象的对比与分析,可得出燃烧需要与氧气接触、温度达到可燃物的着火点.
解答:解:(1)水在通电条件下能分解成氢气和氧气,在电源正极一端产生氧气、电源负极一端产生氢气,且氧气与氢气的体积比约为1:2;
(2)铁丝在氧气中剧烈燃烧,燃烧时火星四射,放出大量的热,生成黑色固体;黑色固体为四氧化三铁,反应的化学方程式为:3Fe+2O2
Fe3O4.
(3)①处铜片传导烧杯中热水的热量使置于铜片上的白磷的温度达到其着火点,并且在其周围有氧气,白磷燃烧;
②处的白磷的温度也达到了其着火点,但由于处于水中而不能与氧气接触,因此没有燃烧;①②对比,可判断燃烧需要有氧气的支持,没有氧气时即使温度达到可燃物的着火点,可燃物也不能燃烧;
③处的红磷虽然处于空气中能与氧气接触,但因温度未能达到其着火点,也没有发生燃烧;①③对比,说明燃烧需要温度达到着火点,温度不能达到着火点时,即使与氧气充分接触,可燃物也不能发生燃烧;
故答案为:(1)氧气;氢气;1:2;
(2)火星四射;3Fe+2O2
Fe3O4
(3)导热;与氧气接触;着火点.
(2)铁丝在氧气中剧烈燃烧,燃烧时火星四射,放出大量的热,生成黑色固体;黑色固体为四氧化三铁,反应的化学方程式为:3Fe+2O2
| ||
(3)①处铜片传导烧杯中热水的热量使置于铜片上的白磷的温度达到其着火点,并且在其周围有氧气,白磷燃烧;
②处的白磷的温度也达到了其着火点,但由于处于水中而不能与氧气接触,因此没有燃烧;①②对比,可判断燃烧需要有氧气的支持,没有氧气时即使温度达到可燃物的着火点,可燃物也不能燃烧;
③处的红磷虽然处于空气中能与氧气接触,但因温度未能达到其着火点,也没有发生燃烧;①③对比,说明燃烧需要温度达到着火点,温度不能达到着火点时,即使与氧气充分接触,可燃物也不能发生燃烧;
故答案为:(1)氧气;氢气;1:2;
(2)火星四射;3Fe+2O2
| ||
(3)导热;与氧气接触;着火点.
点评:燃烧需要同时具有三个条件才能发生:首先要有可燃物,然后还需要与氧气接触、温度达到可燃物的着火点.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目