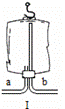题目内容
低碳生活不仅是当今社会的流行语,更是关系到人类未来的战略选择.
(1)“低碳经济”、“低碳生活”的重要含义之一就是节约化石能源,普及利用新能源,以减少二氧化碳的排放.过量排放二氧化碳到大气中,会引起______效应,使全球变暖.
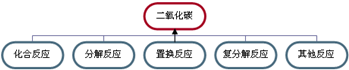
(2)有二氧化碳生成的反应很多(如图所示),请按要求写出一个化学方程式:
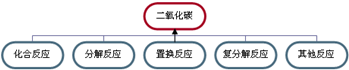
①有二氧化碳生成的分解反应:______;
②有二氧化碳生成的其它反应(不属于基本反应类型):______.
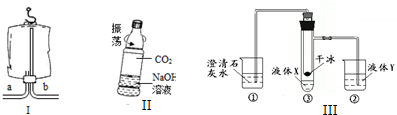
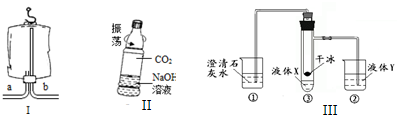
(3)实验室用石灰石(杂质既不溶于水也不与稀盐酸反应)和稀盐酸反应制取二氧化碳.反应的化学方程式为______,若用图I所示医用塑料袋排空气法收集CO2,则CO2导入端为______(填“a”或“b”).
制取二氧化碳实验结束后,锥形瓶内已无气泡产生,但还有少量固体剩余.
小宇对锥形瓶内溶液中溶质的成分进行猜想:
请依小宇的猜想,写出溶液中溶质成分的两种可能______、______.
(4)用图Ⅱ所示矿泉水瓶可以证明CO2与NaOH溶液确实发生了反应,其现象是______,发生的化学方程式为:______.
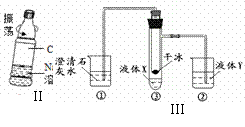
(5)小彤用图Ⅲ装置做以下实验:
打开胶塞向小试管内加入一定量的干冰后将胶塞塞紧.观察到烧杯①中的现象是:______,若液体X为滴加了几滴酚酞的氢氧化钠溶液,液体Y为氯化铁溶液,液体X中发生反应的化学方程式为:______,可能出现的现象有______、______(假设恰好完全反应).
解:(1)过量排放二氧化碳到大气中,会引起温室效应,使全球变暖.
故答案为:温室.
(2)①碳酸在常温下反应生成二氧化碳和水.该反应由一种物质反应生成两种物质,符合分解反应的概念.该反应的化学方程式为:H2CO3═CO2↑+H2O.
②有二氧化碳生成的其他反应(不属于基本反应类型):3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
故答案为:①H2CO3═CO2↑+H2O;②3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
(3)实验室用石灰石和稀盐酸反应制取二氧化碳.反应化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳的密度大于空气的密度,所以用若用图I所示医用塑料袋排空气法收集CO2,则CO2导入端为a;制取二氧化碳实验结束后,锥形瓶内已无气泡产生,但还有少量固体剩余,说明盐酸的量是过量的,则剩余固体完全是杂质,溶液中的溶质是CaCl2和HCl;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;a;CaCl2;HCl.
(4)氢氧化钠能与二氧化碳反应而使瓶内的压强变小,在大气压的作用下,软塑料瓶变瘪,反应方程式是2NaOH+CO2═Na2CO3+H2O.
故答案为:软塑料瓶变瘪;2NaOH+CO2═Na2CO3+H2O.
(5)干冰升华,打开胶塞向小试管内加入一定量的干冰后将胶塞塞紧.观察到①中的现象是有气泡产生;
氯化铁与氢氧化钠反应生成氢氧化铁和氯化钠,然后利用化学方程式书写规则书写即可.FeCl3+3NaOH═Fe(OH)3↓+3NaCl;
氯化钠溶液呈中性,而酚酞遇到酸性和中性溶液显无色,遇到碱性溶液显红色,可能出现的现象有液体Y倒流到液体X中,液体X由红色变为无色或仍为红色.
故答案为:有气泡产生;FeCl3+3NaOH═Fe(OH)3↓+3NaCl;液体Y倒流到液体X中;液体X由红色变为无色或仍为红色.
分析:(1)过量排放二氧化碳到大气中,会引起温室效应;
(2)根据分解反应的含义以及二氧化碳的性质进行解答;
(3)根据石灰石和稀盐酸的反应写出反应的方程式,根据制取二氧化碳的注意事项分析;根据反应物的量进行分析反应后溶液中的溶质;
(4)氢氧化钠能与二氧化碳反应而使瓶内的压强变小;
(1)根据干冰升华以及二氧化碳和氢氧化钙溶液反应生成碳酸钙和水进行解答;
(2)根据氯化铁和氢氧化钠反应生成氯化钠和氢氧化铁,氯化钠溶液呈中性以及酚酞遇到酸性和中性溶液显无色进行解答;
点评:本题主要考查二氧化碳对环境的影响,化学方程式的书写,一些化学现象的分析等知识,以一定的难度.
故答案为:温室.
(2)①碳酸在常温下反应生成二氧化碳和水.该反应由一种物质反应生成两种物质,符合分解反应的概念.该反应的化学方程式为:H2CO3═CO2↑+H2O.
②有二氧化碳生成的其他反应(不属于基本反应类型):3CO+Fe2O3
 2Fe+3CO2;
2Fe+3CO2;故答案为:①H2CO3═CO2↑+H2O;②3CO+Fe2O3
 2Fe+3CO2;
2Fe+3CO2;(3)实验室用石灰石和稀盐酸反应制取二氧化碳.反应化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳的密度大于空气的密度,所以用若用图I所示医用塑料袋排空气法收集CO2,则CO2导入端为a;制取二氧化碳实验结束后,锥形瓶内已无气泡产生,但还有少量固体剩余,说明盐酸的量是过量的,则剩余固体完全是杂质,溶液中的溶质是CaCl2和HCl;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;a;CaCl2;HCl.
(4)氢氧化钠能与二氧化碳反应而使瓶内的压强变小,在大气压的作用下,软塑料瓶变瘪,反应方程式是2NaOH+CO2═Na2CO3+H2O.
故答案为:软塑料瓶变瘪;2NaOH+CO2═Na2CO3+H2O.
(5)干冰升华,打开胶塞向小试管内加入一定量的干冰后将胶塞塞紧.观察到①中的现象是有气泡产生;
氯化铁与氢氧化钠反应生成氢氧化铁和氯化钠,然后利用化学方程式书写规则书写即可.FeCl3+3NaOH═Fe(OH)3↓+3NaCl;
氯化钠溶液呈中性,而酚酞遇到酸性和中性溶液显无色,遇到碱性溶液显红色,可能出现的现象有液体Y倒流到液体X中,液体X由红色变为无色或仍为红色.
故答案为:有气泡产生;FeCl3+3NaOH═Fe(OH)3↓+3NaCl;液体Y倒流到液体X中;液体X由红色变为无色或仍为红色.
分析:(1)过量排放二氧化碳到大气中,会引起温室效应;
(2)根据分解反应的含义以及二氧化碳的性质进行解答;
(3)根据石灰石和稀盐酸的反应写出反应的方程式,根据制取二氧化碳的注意事项分析;根据反应物的量进行分析反应后溶液中的溶质;
(4)氢氧化钠能与二氧化碳反应而使瓶内的压强变小;
(1)根据干冰升华以及二氧化碳和氢氧化钙溶液反应生成碳酸钙和水进行解答;
(2)根据氯化铁和氢氧化钠反应生成氯化钠和氢氧化铁,氯化钠溶液呈中性以及酚酞遇到酸性和中性溶液显无色进行解答;
点评:本题主要考查二氧化碳对环境的影响,化学方程式的书写,一些化学现象的分析等知识,以一定的难度.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目

 更是关系到人类未来的战略选择。
更是关系到人类未来的战略选择。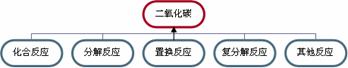
 的现象是: _____________,若液体X为滴加了几滴酚酞的氢氧化钠溶液,液体Y为氯化铁溶液,液体X中发生反应的化学方程式为:________________,可能出现的现象有_________________、______________(假设恰好完全反应)。
的现象是: _____________,若液体X为滴加了几滴酚酞的氢氧化钠溶液,液体Y为氯化铁溶液,液体X中发生反应的化学方程式为:________________,可能出现的现象有_________________、______________(假设恰好完全反应)。