题目内容
【题目】丁基锂( C4H9Li)是橡胶合成工业中一种常用的试剂,白色粉末,熔点﹣95℃,沸点80℃,遇水,空气均易自燃。下列关于丁基锂的说法正确的是( )
A. 丁基锂是由4个碳原子、9个氢原子、1个锂原子构成的
B. 丁基锂中碳元素质量分数为75%
C. 丁基锂运输或使用过程中如果发生燃烧,可以用水浇灭
D. 丁基钾中不含金属元素
【答案】B
【解析】
A、丁基锂是由分子构成的,而不是由原子直接构成的,故选项错误;
B、丁基锂中碳元素质量分数为![]() =75%,故选项正确;
=75%,故选项正确;
C、丁基锂遇水易自燃,所以在运输或使用过程中如果发生燃烧,不能用水浇灭,故选项错误;
D、丁基锂是由碳、氢、锂三种元素组成的,其中锂元素属于金属元素,故选项错误。故选B。

 名校课堂系列答案
名校课堂系列答案【题目】某校化学实验小组的同学们对影响化学反应速率的因素产生了兴趣,为了探究氧化铁能否加快过氧化氢的分解,他们设计了实验装置,并进行气体的制备和测量实验。实验时均以生成40mL气体为标准,相关实验数据记录如表:
实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 过氧化氢溶液温度/℃ | 氧化铁的用量/g | 收集40mL氧气所需时间/s |
① | 5 | 10 | 20 | 0 | 128.5 |
② | 5 | 10 | 20 | 1.2 | 16.8 |
③ | 15 | 10 | 20 | 1.2 | 10.5 |
④ | 5 | 10 | 70 | 0 | 32.7 |
(1)若要证明氧化铁是过氧化氢分解的催化剂,还需要验证它在该反应前后质量和_____未发生改变。请写出过氧化氢在氧化铁的催化下反应的文字表达式:_____,该反应属_____反应(填基本反应类型)
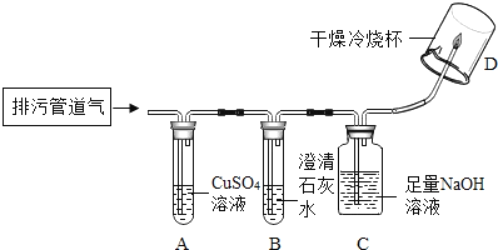
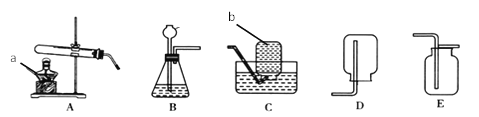
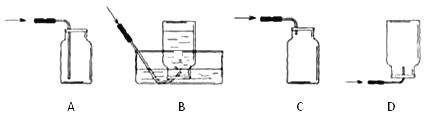
(2)完成上述实验及数据的测定需要用到如图1中的部分装置,请按组装顺序写出所用到的装置代号_____。

(3)用一定量10%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总量_____(选填“减小”“不变”或“增大”)。
(4)通过实验①和④对比可知,温度越高化学反应速率越快,同理通过实验②和③对比可知,得出结论是_____。
查阅资料:将新制的溶质质量分数为5%的过氧化氢溶液,加热到80℃时,才有较多氧气产生,而相同质量5%的过氧化氢溶液加入催化剂,常温下就会立即产生氧气。
(5)采用相同质量5%的过氧化氢溶液,图G虚线表示加热分解制取氧气的曲线,请你在该图2中用实线画出利用催化剂制取氧气的大致曲线(假定两种方法过氧化氢均完全分解)。_________
(6)同学们还想探究催化剂的颗粒大小对化学反应速率是否有影响,请你帮他们设计实验方案进行探究。___________