题目内容
登山队员常用的能源是氢化钙(CaH2)固体,用它和水反应生成氢氧化钙[化学式:Ca(OH)2]和氢气,氢气供燃烧之需。请回答下列问题:
(1)写出氢化钙与水反应的化学方程式_____________________。
(2)现有875 g氢化钙固体(含CaH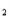 96%),与足量水反应可生成多少克氢气?
96%),与足量水反应可生成多少克氢气?
(1)写出氢化钙与水反应的化学方程式_____________________。
(2)现有875 g氢化钙固体(含CaH
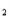 96%),与足量水反应可生成多少克氢气?
96%),与足量水反应可生成多少克氢气?(1) CaH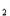 +2H
+2H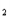 O =Ca( OH)
O =Ca( OH)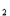 +2H
+2H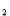 ↑
↑
(2)解:氢化钙的质量为:875 g×96%= 840 g
设生成氢气的质量为x,则:
CaH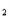 +2H
+2H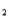 O =Ca(OH)
O =Ca(OH) +2H
+2H ↑
↑
42 4
840 g x
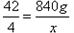 ,
,
解得x=80 g
答:反应可生成80 g氧气。
 +2H
+2H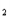 O =Ca( OH)
O =Ca( OH)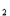 +2H
+2H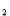 ↑
↑ (2)解:氢化钙的质量为:875 g×96%= 840 g
设生成氢气的质量为x,则:
CaH
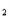 +2H
+2H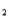 O =Ca(OH)
O =Ca(OH)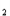 +2H
+2H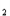 ↑
↑ 42 4
840 g x
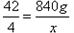 ,
,解得x=80 g
答:反应可生成80 g氧气。

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
