题目内容
元素周期表是学习和研究化学的重要工具,它的内容十分丰富.下表是依据元素周期表画出的1-18号元素的原子结构示意图.我对它进行研究: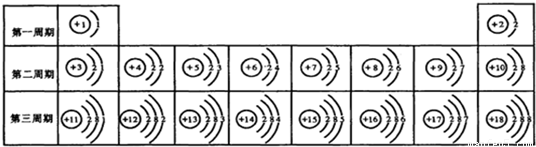
(1)原子序数为17的元素的原子容易______(填“得”或“失”)电子;原子序数为13的元素属于______元素(填“金属”或“非金属”).
(2)原子序数为16的元素与原子序数为______的元素的具有相似的化学性质.
(3)表中不同种元素最本质的区别是______(填番号)
A、质子数不同; B、中子数不同
C、相对原子质量不同; D、电子数不同
(4)根据上面的原子结构示意图推测第7号元素(氮元素)与第14号元素(硅元素)形成的化合物的化学式为______.
(5)元素周期表中每一横行叫一周期,每一竖行叫一族.据上表你估计20号元素应该属于第______族
(6)我发现如下规律:①原子序数与元素原子核电荷数在数值上相等;②______;③______…
(2)根据最外层电子数相同,化学性质相似分析
(3)根据元素的定义分析
(4)根据最外层电子数与化合价的关系分析
(5)根据原子结构示意图中各电子层上电子的排布规律分析
(6)根据原子结构示意图及周期表的特点分析
解答:解:(1)原子序数为17的元素的原子最外层电子数为7,容易 得电子;原子序数为13的元素是铝,带金字旁,属于 金属元素.
(2)原子序数为16的元素最外层上有6个电子,原子序数为 8的元素最外层上也有6个电子,最外层电子数相同,化学性质相似.
(3)元素是具有相同核电荷数的一类原子的总称,不同种元素最本质的区别是质子数不同.故选 A
(4)第7号元素(氮元素)最外层上有5个电子,易得到3个电子,显-3价,第14号元素(硅元素)最外层有4个电子,易失去4个电子,显+4价,二者形成的化合物的化学式为 Si3N4.
(5)根据核外电子排布规律,第一层最多排2个,第二层最多排8个,最外层不能超过8个,因此20号元素最外层上有2个电子,应该属于第 二族
(6)根据原子结构示意图及周期表的排布特点可知每一周期中从左到右原子的最外层电子依次增加1,每一族的原子的最外层电子数相同等;
故答案为:(1)失、金属;(2)8;(3)A;(4)Si3N4;(5)二
(6)每一周期中从左到右原子的最外层电子依次增加1,每一族的原子的最外层电子数相同等
点评:本题考查原子结构示意图及元素周期表中的规律,属于基础知识考查.

 口算题天天练系列答案
口算题天天练系列答案元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
|
族
周期 |
I A |
II A |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 炭 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(1)请从上表中查出关于硼元素的一条信息:___________________________。
(2)请从上表中找出一种元素名称是错误的,更正为 .
(3)第3周期(横行)中属于金属元素的是 (填一种元素符号),其阳离子是 。
(4)在金属活泼性中,镁元素比铝元素活泼,请你从原子结构的观念进行解释 。
(5)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻, 其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水,该反应的化学方程式为 。
元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
|
|
I A |
II A |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(1)请从上表中查出关于硼元素的一条信息: 。
(2)第3周期中相对原子质量最大的金属元素的是 。
(3)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是 (填标号)。
a.C和Ne b.Be和Mg c.Al和Si d.F和Cl
(4)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻,其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体和水,该反应的化学方程式为 。