题目内容
把CO、CO2的混合气体3.4克,通过含有足量氧化铜的试管,反应完全后,将导出的气体全部通入盛有足量石灰水的容器,溶液质量增加了4.4克.
求:
(1)原混合气体中CO的质量?
(2)反应后生成的CO2与原混合气体中CO2的质量比?
解:通过分析可知,混合气中的一氧化碳会与氧化铜中的氧元素生成二氧化碳,增加的质量就是参加反应的氧元素的质量;
设混合气体中CO的质量为x
CO+2CuO 2Cu+CO2 增加的质量
2Cu+CO2 增加的质量
28 44 44-28=16
x 4.4g-3.4g=1g
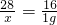
x=1.75g,
(2)混合气体中CO2的质量=3.4g-1.75g=1.65g
生成CO2的质量=4.4g-1.65g=2.75g
(2)反应后生成的CO2与原混合气体中CO2的质量比为:2.75g:1.65g=5:3
答:(1)原混合气体中CO的质量为1.75g
(2)反应后生成的CO2与原混合气体中CO2的质量比为5:3
分析:根据一氧化碳会与氧化铜生成二氧化碳,通过分析可知反应后气体质量增加实际增加的质量就是参加反应的氧元素的质量.
点评:在解此类题时,可以采用反应前后的质量差的方法进行解答.
设混合气体中CO的质量为x
CO+2CuO
 2Cu+CO2 增加的质量
2Cu+CO2 增加的质量28 44 44-28=16
x 4.4g-3.4g=1g
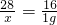
x=1.75g,
(2)混合气体中CO2的质量=3.4g-1.75g=1.65g
生成CO2的质量=4.4g-1.65g=2.75g
(2)反应后生成的CO2与原混合气体中CO2的质量比为:2.75g:1.65g=5:3
答:(1)原混合气体中CO的质量为1.75g
(2)反应后生成的CO2与原混合气体中CO2的质量比为5:3
分析:根据一氧化碳会与氧化铜生成二氧化碳,通过分析可知反应后气体质量增加实际增加的质量就是参加反应的氧元素的质量.
点评:在解此类题时,可以采用反应前后的质量差的方法进行解答.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目