题目内容
【题目】已知:CO2和SO2既有相似性也有差异性.请回答相关问题: 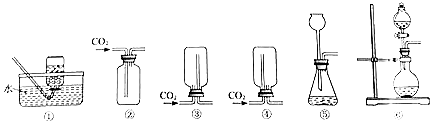
气体 | CO2 | SO2 | |
制备 | 石灰石与盐酸 | Na2SO3与70%硫酸 | |
相似性 | 溶解性 | 能溶于水 | 易溶于水 |
与澄清石灰水反应 | 二者都产生白色浑浊 | ||
差异性 | 与KMnO4溶液 | 不反应 | 气体被吸收,溶液逐渐褪色 |
(1)化石燃料的气体产物中有CO2和SO2等物质,其中SO2是形成的主要物质(填一污染名称).
(2)制取CO2的化学方程式是 , 可用于收集CO2装置是 . (选填如图序号).
(3)写出Na2SO3与70%硫酸反应的化学方程式 , 制备SO2发生装置用 . (选填如图序号).
(4)将收集满SO2的试管倒扣在水中观察到的现象是 .
(5)结合已知信息,请你设计实验证明化石燃料燃烧的气体产物中有CO2(写出操作、试剂、现象、结论) .
【答案】
(1)酸雨
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;②或③
(3)Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;⑥
(4)试管中液面上升
(5)把化石燃料燃烧的气体,先通入足量的KMnO4溶液中,再通入澄清石灰水中,澄清石灰水变浑浊,证明燃烧产物中有二氧化碳
【解析】解:(1)二氧化硫是形成酸雨的主要气体,所以答案是:酸雨;(2)实验室制取CO2 , 是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;可用于收集CO2装置是②或③,因为二氧化碳的密度比空气大;所以答案是:CaCO3+2HCl=CaCl2+H2O+CO2↑;②或③;(3)Na2SO3与70%硫酸常温下反应生成硫酸钠和二氧化硫和水,配平即可,因此不需要加热;所以答案是:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;⑥;(4)将收集满SO2的试管倒扣在水中观察到的现象是:试管中液面上升,因为二氧化硫易溶于水;所以答案是:试管中液面上升;(5)设计实验:把化石燃料燃烧的气体,先通入足量的KMnO4溶液中,再通入澄清石灰水中,澄清石灰水变浑浊,证明燃烧产物中有二氧化碳;所以答案是:把化石燃料燃烧的气体,先通入足量的KMnO4溶液中,再通入澄清石灰水中,澄清石灰水变浑浊,证明燃烧产物中有二氧化碳;
【考点精析】通过灵活运用二氧化碳的检验和验满和书写化学方程式、文字表达式、电离方程式,掌握验证方法:将制得的气体通入澄清的石灰水,如能浑浊,则是二氧化碳.验满方法:用点燃的木条,放在集气瓶口,木条熄灭.证明已集满二氧化碳气体;注意:a、配平 b、条件 c、箭号即可以解答此题.

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案