题目内容

⑴ 根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
⑵ 求该石灰石中碳酸钙的质量分数。(有关反应的化学方程式为:CaCO3+2HCl===CaCl2+H2O+CO2↑)
⑵ 解:设该石灰石样品中碳酸钙的质量为x。
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 44
x 4.4g
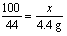
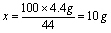
此石灰石中碳酸钙的质量分数为:
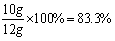

三明市民新水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
|
反应前 |
反应后 |
||
|
实验数据 |
烧杯和稀盐酸的质量 |
石灰石样品的质量 |
烧杯和其中混合物的质量 |
|
150 g |
12 g |
157.6 g |
|
相对原子质量: C 12 O 16 Ca 40
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
(2)求该石灰石中碳酸钙的质量分数。(有关反应的化学方程式为:CaCO3+2HCl==CaCl2+H2O+CO2↑)
(08福建三明)(6分)三明市民新水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
反应前 | 反应后 | ||
实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
150 g | 12 g | 157.6 g | |
相对原子质量: C 12 O 16 Ca 40
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
(2)求该石灰石中碳酸钙的质量分数。(有关反应的化学方程式为:CaCO3+2HCl==CaCl2+H2O+CO2↑)
三明市民新水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
⑴根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
⑵求该石![]() 灰石中碳酸钙的质量分数。
灰石中碳酸钙的质量分数。
(有关反应的化学方程式为:CaCO3+2HCl![]() CaCl2+H2O+CO2↑)
CaCl2+H2O+CO2↑)
