题目内容
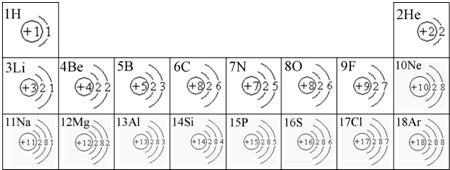
根据元素的原子结构和性质,科学家将元素有序地排列起来,得到元素周期表.(1)以下是部分元素的原子结构示意图:
| H | Li | C | F | Na | Mg | Cl |
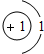 |  | 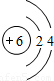 |  |  |  | 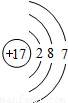 |
 中的“12”表示______,它形成的离子与Cl-形成的化合物中氯元素的化合价为______.
中的“12”表示______,它形成的离子与Cl-形成的化合物中氯元素的化合价为______.(2)下面是元素周期表的一部分(1、2、3周期),从原子结构示意图和周期表可知:主族(纵列)序数等于原子最外层电子数,周期(横行)序数=______.
(3)请用元素符号将碳元素填在周期表的相应位置.
______
| H | |||||||
| Li | F | ||||||
| Na | Mg | ||||||
【答案】分析:(1)根据粒子结构示意图中用圆圈表示原子核,圆圈内的数字表示质子数,判断圆圈内12的表示意义;根据离子符合判断由该离子构成化合物中该元素的化合价;
(2)原子在元素周期表中所处周期序数与该原子的核外电子层数相同;
(3)碳原子核外有2层电子、最外层有4个电子,根据主族(纵列)序数等于原子最外层电子数,周期(横行)序数等于核外电子层数,判断碳元素在同期表中的位置;
(4)根据F原子的结构示意图,判断最外层电子数与F原子相同的原子,该元素的化学性质与F元素化学性质相似.
解答:解:(1)12为该原子核内的质子数,即质子数为12;Cl-带一个单位负电荷,在与镁离子形成的化合物中,氯元素的化合价为-1价;
(2)在元素周期表中,元素所在周期数与该元素的原子核外电子层数相同;
(3)碳原子核外的6个电子分两层排布,且最外层电子数为4,因此,碳元素处于周期表中2周期Ⅳ族;
(4)F原子最外层电子数为7,氯原子最外层电子数也为7,根据原子结构中最外层电子数决定元素的化学性质,F元素的化学性质与Cl元素相似;
故答案为:(1)质子数(或核电荷数)为12;-1;(2)电子层数;(3)2周期Ⅳ族;(4)Cl(或氯).
点评:元素周期表中,同一周期的元素的原子核外电子层数相同;同一族的元素的原子最外层电子数相同,化学性质相似.
(2)原子在元素周期表中所处周期序数与该原子的核外电子层数相同;
(3)碳原子核外有2层电子、最外层有4个电子,根据主族(纵列)序数等于原子最外层电子数,周期(横行)序数等于核外电子层数,判断碳元素在同期表中的位置;
(4)根据F原子的结构示意图,判断最外层电子数与F原子相同的原子,该元素的化学性质与F元素化学性质相似.
解答:解:(1)12为该原子核内的质子数,即质子数为12;Cl-带一个单位负电荷,在与镁离子形成的化合物中,氯元素的化合价为-1价;
(2)在元素周期表中,元素所在周期数与该元素的原子核外电子层数相同;
(3)碳原子核外的6个电子分两层排布,且最外层电子数为4,因此,碳元素处于周期表中2周期Ⅳ族;
(4)F原子最外层电子数为7,氯原子最外层电子数也为7,根据原子结构中最外层电子数决定元素的化学性质,F元素的化学性质与Cl元素相似;
故答案为:(1)质子数(或核电荷数)为12;-1;(2)电子层数;(3)2周期Ⅳ族;(4)Cl(或氯).
点评:元素周期表中,同一周期的元素的原子核外电子层数相同;同一族的元素的原子最外层电子数相同,化学性质相似.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 22、科学家根据元素的原子结构和性质,把它们科学有序地排列起来得到了元素周期表.右图所示为元素周期表的-格,它直接显示了4种信息.其中“22”表示
22、科学家根据元素的原子结构和性质,把它们科学有序地排列起来得到了元素周期表.右图所示为元素周期表的-格,它直接显示了4种信息.其中“22”表示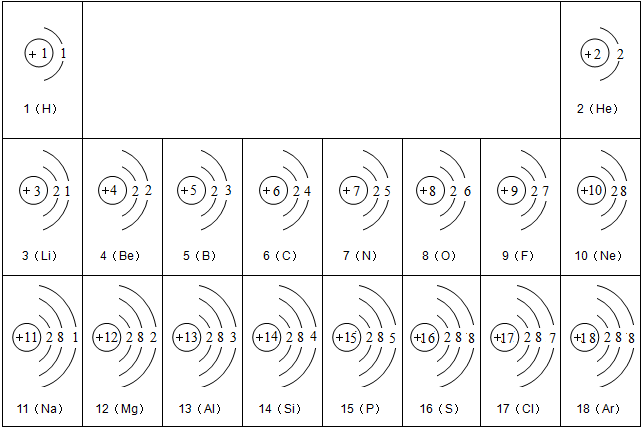









 科学家根据元素的原子结构和性质,把它们科学有序地排列起来得到了元素周期表.图为元素周期表的一格,它直接显示了4种信息.请你指出其中两种,分别是
科学家根据元素的原子结构和性质,把它们科学有序地排列起来得到了元素周期表.图为元素周期表的一格,它直接显示了4种信息.请你指出其中两种,分别是