题目内容
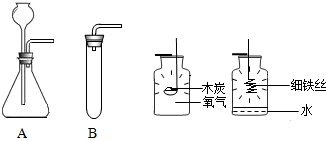
(2013?茂名)同学们在探究物质的性质时,进行了如下实验:
(3)另一个同学利用铜丝、硫酸铝溶液、硝酸银溶液等三种药品以及试管,完成了一个探究实验.请将相应内容填在下表中.
| 编号 | 实验内容与操作 | 实验现象 | 分析与结论 |
| (1) | 分别向盛有NaOH溶液、KOH溶液的A,B两试管中加入CuSO4溶液 | 两支试管均有 蓝色 蓝色 沉淀生成 |
不同的碱溶液都含有 OH- OH- (填化学符号)所以不同的碱都有相似的化学性质 |
| (2) | 用玻璃棒分别蘸取稀 硫酸 硫酸 和浓硫酸 硫酸 于白纸A,B上,片刻. |
白纸A没明显现象;白纸B变黑(生成了炭) | 同种酸,由于 浓度 浓度 不同,它们性质不完全相同 |
| 实验内容与操作 | 实验现象 | 结论 |
分别将铜丝浸入盛有硝酸银、硫酸铝溶液的A、B两试管中 分别将铜丝浸入盛有硝酸银、硫酸铝溶液的A、B两试管中 |
试管A中的铜丝表面有银白色物质生成,溶液逐渐变蓝色,试管B无明显现象 试管A中的铜丝表面有银白色物质生成,溶液逐渐变蓝色,试管B无明显现象 |
金属活动性顺序:Al>Cu>Ag 金属活动性顺序:Al>Cu>Ag |
分析:(1)根据碱溶液的化学性质分析
(2)根据浓硫酸的脱水性分析
(3)根据探究金属活动性实验所需药品分析
(2)根据浓硫酸的脱水性分析
(3)根据探究金属活动性实验所需药品分析
解答:解:(1)NaOH、KOH溶液中都含有氢氧根离子,都能与CuSO4溶液中的铜离子结合成氢氧化铜蓝色沉定,由此可知不同的碱溶液具有相似化学性质的原因是因为溶液中都含有氢氧根离子.
(2)浓硫酸具有脱水性,白纸上沾上浓硫酸会变黑,稀硫酸没有脱水性,不会使白纸变黑.浓硫酸和稀硫酸浓度不同,决定了性质不同.
(3)给定物质为一种金属两种盐溶液,可将铜丝浸入盛有硝酸银、硫酸铝溶液的A、B两试管中,可观察到试管A中的铜丝表面有银白色物质生成,溶液逐渐变蓝色,试管B无明显现象,由此可探究三种金属:铝、铜、银的金属活动性顺序为Al>Cu>Ag
故答案为:
(3)
(2)浓硫酸具有脱水性,白纸上沾上浓硫酸会变黑,稀硫酸没有脱水性,不会使白纸变黑.浓硫酸和稀硫酸浓度不同,决定了性质不同.
(3)给定物质为一种金属两种盐溶液,可将铜丝浸入盛有硝酸银、硫酸铝溶液的A、B两试管中,可观察到试管A中的铜丝表面有银白色物质生成,溶液逐渐变蓝色,试管B无明显现象,由此可探究三种金属:铝、铜、银的金属活动性顺序为Al>Cu>Ag
故答案为:
| (1) | 蓝色 | OH- | |
| (2) | 硫酸硫酸 | 浓度 |
| 分别将铜丝浸入盛有硝酸银、硫酸铝溶液的A、B两试管中 | 试管A中的铜丝表面有银白色物质生成,溶液逐渐变蓝色,试管B无明显现象 | 金属活动性顺序:Al>Cu>Ag |
点评:本题考查碱的化学性质、浓硫酸的脱水性以及金属活动性顺序的实验探究,属中档题目.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
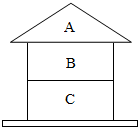 (2013?抚顺)同学们以盖房子的方式总结出了如下物质间的关系.A、B、C均为纯净物,且上、下相邻的物质间均可发生反应.回答下列问题.
(2013?抚顺)同学们以盖房子的方式总结出了如下物质间的关系.A、B、C均为纯净物,且上、下相邻的物质间均可发生反应.回答下列问题.