题目内容
【题目】室温时,随着向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化),下列分析正确的是( )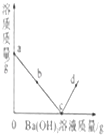
A.a点溶液中有两种溶质
B.b点溶液中滴加紫色石蕊溶液,溶液变蓝
C.c点烧杯内液体的pH=7
D.d点溶液中较多的Ba2+、OH﹣、SO42﹣、H+
【答案】C
【解析】A、a点时,反应没有开始,溶液中有一种溶质H2SO4 , 故错误;
B、稀H2SO4与Ba(OH)2溶液的反应生成硫酸钡沉淀和水,溶质质量减小,c点完全反应,b点溶液中有硫酸,滴加紫色石蕊溶液,溶液变红,故错误;
C、稀H2SO4与Ba(OH)2溶液的反应生成硫酸钡沉淀和水,溶质质量减小,完全反应后,溶质质量为0,c点完全反应,杯内液体的pH=7,故正确;
D、完全反应后继续加Ba(OH)2溶液到d点,点d溶液中较多的Ba2+、OH﹣ , 无SO42﹣、H+ , 故错误.
答案:C.
A、根据a点时,反应没有开始,溶液中有一种溶质H2SO4解答;B、根据稀H2SO4与Ba(OH)2溶液的反应生成硫酸钡沉淀和水,b点溶液中有硫酸解答;C、根据稀H2SO4与Ba(OH)2溶液的反应生成硫酸钡沉淀和水,溶质质量减小,c点表示完全反应解答;D、根据完全反应后继续加Ba(OH)2溶液到d点解答.此题是多个知识点的考查题,能对多个物质的反应过程达到有效分析,并能结合读懂图象是解题的关键.

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】科学兴趣小组学习二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
①选择装置并检查气密性.
②称取0.1g的二氧化锰粉末加入容器中.
③量取20毫升溶质质量分数约1%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
④改变二氧化锰的质量,重复上述实验,记录数据如表.
时间/秒 | 生成氧气的体积/毫升 | |||
0.1g MnO2 | 0.2g MnO2 | 0.3g MnO2 | 0.4g MnO2 | |
40 | 49 | 61 | 75 | 86 |
80 | 77 | 87 | 90 | 92 |
120 | 89 | 92 | 92 | 92 |
160 | 92 | 92 | 92 | 92 |
(1)本实验探究的问题是 . 从表中数据分析得出的结论是 .
(2)写出实验室用过氧化氢溶液制取氧气反应的文字表达式 .
(3)对于有气体生成的反应,要准确比较反应速率的快慢,除上述方法外,你还可以采用的方法是 .
(4)为了完成本实验应选用的收集装置是 . (填序号)
(5)对于催化剂对化学反应速率的影响还有哪些因素,你可以大胆提出猜想,并设计实验进行验证.(要求仍以过氧化氢分解为例)
你的猜想: .
你的实验设计:(要有实验操作步骤、现象和结论)
步骤:
现象和结论: .
