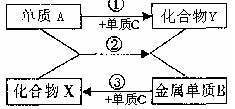
题目内容
氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。
【阅读资料】
①碱石灰是氧化钙和氢氧化钠的混合物;
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气;
③氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
【氢化钙的制备】
氢化钙通常用氢气与钙加热制得。某化学兴趣小组设计的制取装置如图1所示(固定装置省略)。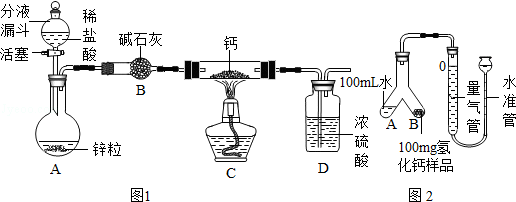
回答下列问题:
(1)装置A中制取氢气的化学方程式为 。
(2)装置B的作用是 。
(3)装置C中制取氢化钙的化学方程式为 。
(4)若不改变温度,整套装置气密性的检查方法是 。
【产品的定量测定】
通过上述方法制得的氢化钙样品中常混有未完全反应的钙(其余可能的杂质忽略不计)。样品纯度的测定步骤如下:
①检查装置气密性,装入药品,按图2(固定装置省略)所示连接仪器;
②调整水准管高度,使量气装置两边的液面保持同一水平。读取液面所在的刻度数据为10.0mL;
③将Y形管慢慢倾斜,直到A端的水全部与B端的样品混合;
④反应结束,冷却至室温,再次读取液面所在刻度数据为110.0mL。
回答下列问题:
(5)如何判断样品与水完全反应: 。
(6)反应生成氢气的体积为 mL。
(7)已知该实验条件下,氢气的密度为0.09mg/mL,样品中氢化钙的纯度为 (结果精确到0.1%)。
(1)Zn+2HCl=ZnCl2+H2↑ (2) 吸收水蒸气和部分氯化氢气体 (3)Ca+H2 CaH2;
CaH2;
(4)将活塞关闭后,往分液漏斗中加入适量的水,用手指堵住装置D的导管口,打开活塞,若气密性良好,可观察到分液漏斗内的液面几乎不下降(合理答案均可);
(5)量气管中液面不再变化(合理答案均可);(6)100.0; (7)88.4%
解析试题分析:(1)依据锌粒与稀盐酸反应原理书写方程式。锌粒与稀盐酸反应生成氯化锌和氢气,反应的方程式是:Zn+2HCl=ZnCl2+H2↑;
(2)根据碱石灰的成分和其中物质的性质分析解答。碱石灰是氧化钙和氢氧化钠的混合物,氧化钙与水可反应,氢氧化钠可作干燥剂,且与盐酸能反应,所以该装置的作用是吸收水蒸气和部分氯化氢气体;
(3)依据反应物、生成物和反应条件书写方程式。钙和氢气在加热的条件下生成氢化钙,方程式是Ca+H2 CaH2;
CaH2;
(4)根据检查装置气密性的方法和题目要求分析解答。要检查该套装置的气密性,可以将活塞关闭后,往分液漏斗中加入适量的水,然后用手指堵住装置D的导管口,打开活塞,观察分液漏斗内的液面变化判断装置是否漏气;
(5)根据装置特点和氢化钙与水反应生成氢气进行分析。由于氢化钙与水反应生成氢气,所以判断样品与水是否完全反应,可以观察右边的量气管中液面,若不再变化,则已完全反应;
(6)氢气的体积等于反应前后液面差,为:110.0mL﹣10.0mL=100.0mL;
(7)依据氢气的质量=氢气的体积×氢气的密度求出氢气的质量,再结合氢化钙与水反应方程式及钙与水反应方程式,求出氢化钙的质量,进而计算样品中氢化钙的纯度。反应生成氢气的质量是:100.0mL×0.09mg/mL=9mg。设样品中氢化钙的质量是X,生成氢气质量为Y,则钙的质量为100mg﹣X,钙与水反应生成氢气质量为9mg﹣Y,则
CaH2+2H2O=Ca(OH)2+2H2↑
42 4
X Y =
=
解得Y=
Ca+2H2O=Ca(OH)2+H2↑
40 2
100mg﹣X 9mg﹣Y
根据: =
=
将Y= 代入
代入
解得X=88.4mg
所以样品中氢化钙的纯度为: ×100%=88.4%。
×100%=88.4%。
考点:考查常用气体的发生装置和收集装置与选取方法

人教版新课标化学教材九年级上册 “分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁(Fe2O3)粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| Ⅱ待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物进行分离,并将所得氧化铁粉末进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
| Ⅳ分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 | |
(1)在第Ⅲ步中,要使剩余物分离必须进行的操作是 ,必须用到的仪器有铁架台、玻璃棒、烧杯和 ,玻璃棒的作用是 。
 (2)在第Ⅳ步实验中,可以用点滴板(如右图所示)代替试管C、D完成,
(2)在第Ⅳ步实验中,可以用点滴板(如右图所示)代替试管C、D完成,改进后的优点是 。
【实验结论】
(1)实验Ⅱ和Ⅲ分别可以证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(2)写出实验Ⅰ的A试管中发生反应的的符号表达式 。
【实验评价】
实验设计Ⅳ的目的是 ;
若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
【知识拓展】
(1)查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是 。
A. 催化剂只加快化学反应速率
B.同一个化学反应可以有多种催化剂
C. MnO2只能作过氧化氢溶液分解的催化剂
D.用作催化剂的物质不可能是其他反应的反应物或生成物
(2) 马铃薯长期放置后会发芽,发芽马铃薯中含有一种致毒成分茄碱(C45H73O15N),又称马铃薯毒素,是一种弱碱性的甙生物碱,又名龙葵甙,大量食用未成熟或发芽马铃薯可引起急性中毒。
①茄碱的相对分子质量为 ;
②茄碱中氢、氧两种元素的元素质量比为 ;
③茄碱中氧元素的质量分数为 (计算结果保留一位小数);
④433.5g茄碱中含有 g碳元素。
过氧化钠是化学中常见的一种药品,它是浅黄白色颗粒粉末.在空气中吸收水分和二氧化碳。易溶于水,与水中能发生反应生成氢氧化钠和过氧化氢,方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能分解放出氧气。
(1)区分水和过氧化氢的实验方法是: ,发生的反应方程式是: .
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究.
提出问题:什么导致溶液先变红再褪色?
猜想与假设:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”.
实验与结论:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为 ;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量稀氢氧化钠溶液于试管中,滴加1﹣2滴酚酞试液,变红后 观察现象 | 溶液依然为红色 | |
讨论交流:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分.(化学试卷总分不超过60分)
猜想3:
方案3:
| 实验步骤 | 实验现象 | 实验结论 |
| | | |
化学实验室开放日,小池和小航同学在药品柜中发现一瓶淡黄色粉末,瓶外贴有“过氧化钠(Na2O2)”的标签,这种外观与硫黄相似的物质到底有哪些性质?他们十分好奇,为了弄清它的有关性质,在老师的指导下,他们进行了以下探究活动:
[查阅资料]过氧化钠(Na2O2)在常温下能与水反应生成氢氧化钠和氧气.氢氧化钠能使无色酚酞试液变红色。
[设计实验]过氧化钠与水反应
[进行实验]
| 实验步骤 | 实验现象 | 结论 |
| 1.在试管中加入适量过氧化钠,再加入足量水; | 1.黄色粉末溶解,有 产生 | 产物 (填“有”或“没有”)氧气; |
| 2.用 伸入试管 | 2.木条复燃 | |
| ③再向试管中加入几滴酚酞试液. | | 产物有氢氧化钠 |
某校化学兴趣小组将用剩的过氧化氢溶液倒入放有生锈铁钉的废液缸中,发现产生了大量的气泡,经检验此气体为氧气.根据学过的知识初步判断,是生锈铁钉中的某种物质加快了过氧化氢的分解,那么究竟是哪种物质加快了过氧化氢的分解速率?请你参与他们的研究,分享和体验探究实验的快乐.
[猜想与假设]
甲同学:铁钉表面的氧化铁加快了H2O2的溶液分解.
乙同学:铁钉里的 加快了H2O2的溶液分解.
[设计方案和实验] 完成下列表格
| 实验方案 | 实验现象 | 结论 |
| 方案一:向盛有10mL 5% H2O2溶液的试管中 加入2g氧化铁粉末,将一根带火星的木条放 在试管口,观察现象. | | 甲同学结论成立. |
| 方案二:向盛有10mL 5% H2O2溶液的试管中加入 粉末,将一根带火星的木条放在试管口,观察现象. | | 乙同学结论 . (填“成立”或“不成立”) |
(提示:下面小题若答对将奖励4分,但化学总分不超过60分.)
[反思与评价] 丁同学仔细观察“方案二”中一直没有现象的试管,过了一段时间后发现试管中也产生了气体,丁同学对此现象进行深入思考和分析,得出可能的原因,你能想出其中的原因吗? 。
我国第四套人民币硬币中使用到镍(Ni)、铜、铁等金属.某兴趣小组决定探究Ni、Fe、Cu的金属活动性顺序.
(1)【查阅资料】
镍能与盐酸或稀硫酸反应,生成可溶于水的正二价镍盐,并放出氢气.
①写出镍与盐酸反应的化学方程式 .
②结合所学知识, (填“能”或“不能”)直接比较出Ni、Fe的金属活动性强弱.
(2)【探究实验】(所用金属片均已用砂纸打磨.)
| 实验步骤 | 实验现象 | 实现结论 |
 相同浓度的NiSO4 | 铁片表面有固体析出,铜片表面 . | 三种金属活动性由强到弱的顺序为 . |
(3)【迁移应用】
用镍片、硫酸亚铁溶液和 溶液通过实验也能判断Fe、Ni、Cu的金属活动性顺序.
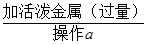 金属混合物+溶液A
金属混合物+溶液A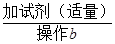 单质银
单质银