题目内容
海水资源的利用具有非常广阔的前景.(1)海水的潮起潮落蕴含巨大的能量,潮汐能和 (写一种)属于新能源.海底矿产“可燃冰”的开发产品与天然气的主要成份相同,是 (写化学式)
(2)海水淡化是解决淡水资源危机的有效途径之一,下列水的净化方法中,能使海水淡化的是 (填序号,下同).
①过滤 ②吸附 ③蒸馏 ④消毒
(3)从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和传热介质,重水中的D原子核内有一个质子、一个中子,下列说法正确的是 .
①D原子与氢原子属于同种元素 ②重水的相对分子质量为18
③D原子核外有一个电子 ④D原子的相对原子质量为2
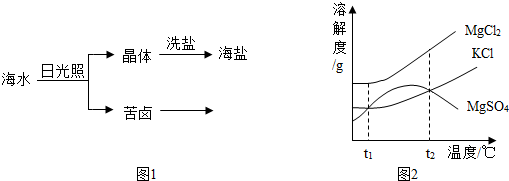
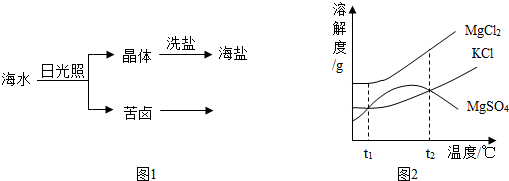
(4)海水中含有多种盐,如氯化钠、氯化镁等.海水晒盐大致经历图1所示的过程
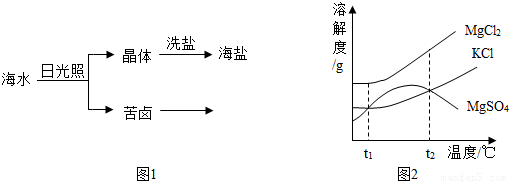
①图2是苦卤中有关物质的溶解度曲线,已知t1℃时,氯化镁和氯化钾的溶解度分别为M、N,则它们溶解度大小的关系为 :将苦卤加热到t2℃以上,根据溶解度曲线,首先析出的晶体应是 .
②在晒盐时,海水中的氯化镁等也有少量结晶析出,所以海盐生产要经历用饱和食盐水洗盐的过程,采用饱和食盐水做洗液的原因是 .
【答案】分析:(1)根据人们对能源利用的科技程度分类分析解答;天然气的主要成分是甲烷;
(2)根据水的净化方法的原理分析解答;
(3)根据元素种类判断方法,相对分子质量及相对原子质量的计算方法等分析解答;
(4)①根据溶解度曲线可以比较同一温度时物质的溶解度大小;看出物质的溶解度受温度的影响情况,从而确定析出晶体的情况;
②饱和溶液是一定温度下,一定量的溶剂里不能继续溶解某种溶质的溶液.
解答:解:(1)根据人们对能源利用的科技程度可将能源分为:常规能源,新能源,是指尚未大规模商业应用,在技术、经济上进一步研究的、有前途的能源,例如,太阳能、风能、潮汐能、地热能、和核能等;天然气的主要成分是甲烷,其化学式是CH4;
故答案为:太阳能(合理均可);CH4;
(2)海水淡化是去除水中的氯化钠、氯化镁等可溶性盐,转化为淡水的方法;
①过滤是除去不溶性杂质的方法,不能除去水中的可溶性物质,故错误;
②吸附是除去水中色素、异味等不溶性杂质的一种方法,不能除去水中的氯化钠、氯化镁等可溶性盐,故错误;
③蒸馏是通过加热的方法将水变成水蒸气,再冷凝成水的方法,可以得到最纯的蒸馏水,故可将水淡化,正确;
④消毒是杀死水中的细菌、微生物的方法,不能除去水中的氯化钠、氯化镁等可溶性盐,故错误;
故选③;
(3)①元素的种类是由质子数决定的,D原子与氢原子都含有一个质子,属于同种元素,正确;
②相对原子质量=质子数+中子数,所以D原子的相对原子质量=1+1=2;则重水的相对分子质量为:2×2+16=20,故题目错误;
③原子中质子数=电子数,D原子核内有一个质子,所以核外有一个电子,正确;
④由②可知:D原子的相对原子质量为2,正确;
故选①③④;
(4)①t1℃时,氯化镁的溶解度大于氯化钾的溶解度,即M>N;将苦卤加热到t2℃以上,根据溶解度曲线,可以看出,硫酸镁的溶解度随温度的升高先增大后减小,而氯化钠和氯化镁的溶解度随温度的升高溶解度逐渐增大,所以首先析出的晶体应是硫酸镁;
故答案为:M>N;硫酸镁;
②要去掉氯化钠中的氯化镁等少量晶体,用饱和食盐水做洗液的原因是:饱和食盐水能溶解氯化镁等其他盐,但不溶解食盐,可以最大程度的减少食盐的损失;
故答案为:饱和食盐水能溶解氯化镁等其他盐,但不溶解食盐,可以最大程度的减少食盐的损失.
点评:本题综合的考查了学生水的净化方法的原理,溶解度曲线的应用,原子的相关内容等知识,解答时要结合所学知识细心分析.
(2)根据水的净化方法的原理分析解答;
(3)根据元素种类判断方法,相对分子质量及相对原子质量的计算方法等分析解答;
(4)①根据溶解度曲线可以比较同一温度时物质的溶解度大小;看出物质的溶解度受温度的影响情况,从而确定析出晶体的情况;
②饱和溶液是一定温度下,一定量的溶剂里不能继续溶解某种溶质的溶液.
解答:解:(1)根据人们对能源利用的科技程度可将能源分为:常规能源,新能源,是指尚未大规模商业应用,在技术、经济上进一步研究的、有前途的能源,例如,太阳能、风能、潮汐能、地热能、和核能等;天然气的主要成分是甲烷,其化学式是CH4;
故答案为:太阳能(合理均可);CH4;
(2)海水淡化是去除水中的氯化钠、氯化镁等可溶性盐,转化为淡水的方法;
①过滤是除去不溶性杂质的方法,不能除去水中的可溶性物质,故错误;
②吸附是除去水中色素、异味等不溶性杂质的一种方法,不能除去水中的氯化钠、氯化镁等可溶性盐,故错误;
③蒸馏是通过加热的方法将水变成水蒸气,再冷凝成水的方法,可以得到最纯的蒸馏水,故可将水淡化,正确;
④消毒是杀死水中的细菌、微生物的方法,不能除去水中的氯化钠、氯化镁等可溶性盐,故错误;
故选③;
(3)①元素的种类是由质子数决定的,D原子与氢原子都含有一个质子,属于同种元素,正确;
②相对原子质量=质子数+中子数,所以D原子的相对原子质量=1+1=2;则重水的相对分子质量为:2×2+16=20,故题目错误;
③原子中质子数=电子数,D原子核内有一个质子,所以核外有一个电子,正确;
④由②可知:D原子的相对原子质量为2,正确;
故选①③④;
(4)①t1℃时,氯化镁的溶解度大于氯化钾的溶解度,即M>N;将苦卤加热到t2℃以上,根据溶解度曲线,可以看出,硫酸镁的溶解度随温度的升高先增大后减小,而氯化钠和氯化镁的溶解度随温度的升高溶解度逐渐增大,所以首先析出的晶体应是硫酸镁;
故答案为:M>N;硫酸镁;
②要去掉氯化钠中的氯化镁等少量晶体,用饱和食盐水做洗液的原因是:饱和食盐水能溶解氯化镁等其他盐,但不溶解食盐,可以最大程度的减少食盐的损失;
故答案为:饱和食盐水能溶解氯化镁等其他盐,但不溶解食盐,可以最大程度的减少食盐的损失.
点评:本题综合的考查了学生水的净化方法的原理,溶解度曲线的应用,原子的相关内容等知识,解答时要结合所学知识细心分析.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目