题目内容
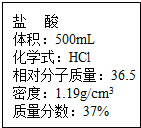 实验室保存一瓶浓盐酸,瓶上标签的部分内容如图所示,请你根据标签上提供的数据计算:(计算结果精确到0.01)
实验室保存一瓶浓盐酸,瓶上标签的部分内容如图所示,请你根据标签上提供的数据计算:(计算结果精确到0.01)(1)瓶内浓盐酸溶质的质量是多少?
(2)用5mL浓盐酸可以配制溶质质量分数为10%的盐酸多少克?
(3)实验室用182.5g质量分数为10%的稀盐酸和足量的大理石充分反应,可生成CO2的质量为多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据标签上提供的数据可以计算瓶内浓盐酸溶质的质量;
(2)溶液稀释前后,溶质质量不变;
根据盐酸的质量可以计算生成二氧化碳的质量.
(2)溶液稀释前后,溶质质量不变;
根据盐酸的质量可以计算生成二氧化碳的质量.
解答:解:(1)瓶内浓盐酸溶质的质量为:1.19g/cm3×500mL×37%=220.15g,
答:瓶内浓盐酸溶质的质量为220.15g.
(2)用5mL浓盐酸可以配制溶质质量分数为10%的盐酸质量为:(1.19g/cm3×5mL×37%)÷10%=22.02g,
答:用5mL浓盐酸可以配制溶质质量分数为10%的盐酸质量为22.02g.
(3)设生成二氧化碳的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
182.5g×10% x
=
,
x=11g,
答:生成二氧化碳的质量为11g.
答:瓶内浓盐酸溶质的质量为220.15g.
(2)用5mL浓盐酸可以配制溶质质量分数为10%的盐酸质量为:(1.19g/cm3×5mL×37%)÷10%=22.02g,
答:用5mL浓盐酸可以配制溶质质量分数为10%的盐酸质量为22.02g.
(3)设生成二氧化碳的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
182.5g×10% x
| 73 |
| 182.5g×10% |
| 44 |
| x |
x=11g,
答:生成二氧化碳的质量为11g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
下列实验方法中错误的是( )
| A、用酚酞溶液检验氢氧化钠是否变质 |
| B、用肥皂水区分硬水和软水 |
| C、用灼烧的方法鉴别羊毛和涤纶 |
| D、用带火星木条伸入集气瓶内检验二氧化碳气体 |
下列说法正确的是( )
| A、石蕊溶液可鉴别石灰水和氢氧化钠溶液 |
| B、除去碳粉中的CuO可用稀硫酸 |
| C、由化学方程式SiO2+2C═Si+2R↑可知R为CO2 |
| D、酸雨与SO2、CO2有关 |
微型新录音录像的高性能带中磁粉主要材料之一是化学组成丰当于CoFe2O4的化合物,若钴为+2价,则铁的化合价为( )
| A、+3 | B、+2 | C、-2 | D、-3 |

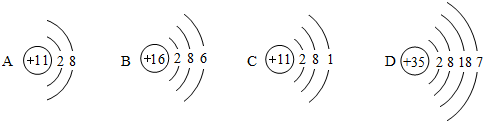
 ,则x的数值可能是下列中的
,则x的数值可能是下列中的