题目内容
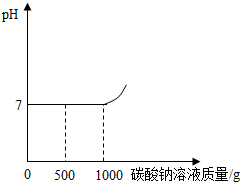 (2013?丰台区二模)做完“二氧化碳的制取和性质”实验后,废液桶中有大量盐酸与氯化钙的混合溶液(不考虑其他杂质).为避免污染环境并回收利用废液,化学兴趣小组同学们做了如下实验:取废液桶中上层清液522g,加入足量的CaCO3粉末,生成22g气体,过滤,得到a g滤液.向滤液中加入溶质质量分数为21.2%的碳酸钠溶液,所得溶液pH与加入的碳酸钠溶液的质量关系如图所示.查阅资料:Na2CO3+CaCl2=CaCO3↓+2NaCl.
(2013?丰台区二模)做完“二氧化碳的制取和性质”实验后,废液桶中有大量盐酸与氯化钙的混合溶液(不考虑其他杂质).为避免污染环境并回收利用废液,化学兴趣小组同学们做了如下实验:取废液桶中上层清液522g,加入足量的CaCO3粉末,生成22g气体,过滤,得到a g滤液.向滤液中加入溶质质量分数为21.2%的碳酸钠溶液,所得溶液pH与加入的碳酸钠溶液的质量关系如图所示.查阅资料:Na2CO3+CaCl2=CaCO3↓+2NaCl.(1)a的值为
550
550
.(2)加入1000g碳酸钠溶液充分反应后,所得溶液要配制成16%的溶液用于农业选种,需加水多少.
分析:(1)根据生成的二氧化碳气体的质量可以计算出消耗的碳酸钠的质量,进而结合质量守恒定律可以计算出a的值;
(2)根据消耗的碳酸钠的质量,结合反应的化学方程式可以计算出反应后得到的氯化钠溶液的质量分数,然后根据稀释前后溶质的质量不变来完成解答即可.
(2)根据消耗的碳酸钠的质量,结合反应的化学方程式可以计算出反应后得到的氯化钠溶液的质量分数,然后根据稀释前后溶质的质量不变来完成解答即可.
解答:解:(1)设生成22g气体消耗碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 22g
=
解得x=50g
所以a=522g+50g-22g=550g
(2)设生成氯化钠的质量为y,碳酸钙的质量为z,加水质量为b.
m(Na2CO3)=1000 g?21.2%=212 g
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
212g z y
=
=
解得:y=234g;z=200g;
所得氯化钠溶液的溶质的质量分数为:
×100%=16%
b=112.5g
答:需加水112.5g.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 22g
| 100 |
| x |
| 44 |
| 22g |
解得x=50g
所以a=522g+50g-22g=550g
(2)设生成氯化钠的质量为y,碳酸钙的质量为z,加水质量为b.
m(Na2CO3)=1000 g?21.2%=212 g
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
212g z y
| 106 |
| 212g |
| 100 |
| z |
| 117 |
| y |
解得:y=234g;z=200g;
所得氯化钠溶液的溶质的质量分数为:
| 234g |
| 550g+1000g-200g+b |
b=112.5g
答:需加水112.5g.
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地解答即可.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
 (2013?丰台区二模)某脱氧保鲜剂主要成分为活性铁粉(如图所示),利用铁与氧气、水反应生成氢氧化铁的性质来吸收包装袋内氧气,从而延长食品的保质期.已知该脱氧保鲜剂中活性铁粉的质量为1.4g,理论上该脱氧保鲜剂最多能够吸收氧气的质量为( )
(2013?丰台区二模)某脱氧保鲜剂主要成分为活性铁粉(如图所示),利用铁与氧气、水反应生成氢氧化铁的性质来吸收包装袋内氧气,从而延长食品的保质期.已知该脱氧保鲜剂中活性铁粉的质量为1.4g,理论上该脱氧保鲜剂最多能够吸收氧气的质量为( )