题目内容
【题目】向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图。
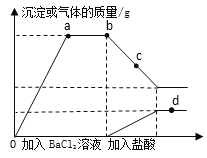
①写出0a过程中的发生反应的一个化学方程式_____________,反应类型________。
②加入盐酸b→c的现象是______________。
③c点溶液中含有的溶质是_____________。
④a、b、c、d四点所含BaCl2的质量关系是________(用“>”、“<”或“=”表示)。
【答案】 Na2CO3 +BaCl2 =2NaCl+BaCO3 ↓(或Na2SO4 +BaCl2 =2NaCl+BaSO4 ↓) 复分解反应 沉淀部分溶解,有气泡产生 NaCl、BaCl2 d>c>b>a
【解析】① BaCl2溶液与Na2CO3、Na2SO4都能发生反应生成沉淀,由两种化合物互相交换成分,生成另外两种化合物的反应是复分解反应。②盐酸能与产生的BaCO3反应,生成可溶性的BaCl2 ,同时生成二氧化碳气体,而BaSO4不溶于盐酸,故实验现象是沉淀部分溶解,有气泡产生。③ Na2CO3 +BaCl2 =2NaCl+BaCO3 ↓ Na2SO4 +BaCl2 =2NaCl+BaSO4 ↓,沉淀除外生成物都是氯化钠,BaCO3+ 2HCl== BaCl2 +CO2↑+H2O ,生成可溶性的BaCl2,故 c 点溶液中含有的溶质是NaCl、BaCl2 。④a点时BaCl2溶液与Na2CO3、Na2SO4混合溶液恰好反应,然后继续滴加BaCl2溶液,故b>a,c点是加入的盐酸与部分BaCO3反应,生成可溶性的BaCl2 ,故c>b,d点时,碳酸钡已经完全与盐酸反应生成了可溶性的BaCl2,故 d>c>b>a。

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目