题目内容
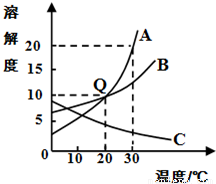
如图是A、B、C三种物质的溶解度曲线,据图回答:(1)30℃时,A、B、C三种物质的溶解度由小到大的顺序是 (填写序号);
(2)要使接近饱和的A物质溶液变为饱和,可采取的一种措施是 ;
(3)20℃时,将A物质40g加入到50g水中充分搅拌,形成溶液的质量是 g;
(4)30℃时,取等质量A、B、C三种物质的饱和溶液,温度降至10℃时,所得溶液的溶质质量分数由大到小的顺序为 (填写序号).
【答案】分析:(1)由溶解度曲线图可以比较同一温度时物质的溶解度大小;
(2)A物质的溶解度受温度的影响较大,随温度的升高而增大,不饱和溶液变为饱和溶液可采取增加溶质、降低温度的方法,据此分析解答;
(3)20℃时 A物质的溶解度为10g,即100g水最多能溶解10gA物质,据此分析;
(4)由溶解度曲线图可以看出,在30℃时ABC的溶解度关系为A>B>C,根据饱和溶液中溶质质量分数的计算公式 ×100%,可以判断此时饱和溶液中质量分数关系为A>B>C,降温后A、B溶液中均有晶体析出,还是饱和溶液,但在10℃时,A的溶解度比B小,所以此时溶质质量分数为:B>A,C的溶解度随温度降低而升高变为不饱和溶液,则溶质质量分数将不变,最后进行综合比较得出答案.
×100%,可以判断此时饱和溶液中质量分数关系为A>B>C,降温后A、B溶液中均有晶体析出,还是饱和溶液,但在10℃时,A的溶解度比B小,所以此时溶质质量分数为:B>A,C的溶解度随温度降低而升高变为不饱和溶液,则溶质质量分数将不变,最后进行综合比较得出答案.
解答:解:(1)由溶解度曲线图可以看出,在30℃时A、B、C三种物质的溶解度由小到大的顺序是C、B、A;
(2)A物质的溶解度受温度的影响较大,随温度的升高而增大,故可采用降温或加入溶质的方法使其变为饱和溶液;
(3)20℃时 A物质的溶解度为10g,即100g水最多能溶解10gA物质,所以将A物质40g加入到50g水中充分搅拌,可得50g水最多溶解5gB物质,所形成溶液的质量是55g;
(4)由溶解度曲线图可以看出,在30℃时ABC的溶解度关系为A>B>C,可以判断此时其质量分数关系为A>B>C,降温后A、B溶液中均有晶体析出,还是饱和溶液,但在10℃时,A的溶解度比B小,所以此时溶质质量分数为:B>A,C的溶解度随温度降低而升高变为不饱和溶液,则溶质质量分数将不变,故所得溶液的溶质质量分数由大到小的顺序是BAC;
故答案为:(1)C、B、A;(2)加入A物质或降低温度;(3)55;(4)B、A、C.
点评:本题主要考查了固体溶解度曲线所表示的意义,饱和溶液和不饱和溶液的相互转化等知识,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力
(2)A物质的溶解度受温度的影响较大,随温度的升高而增大,不饱和溶液变为饱和溶液可采取增加溶质、降低温度的方法,据此分析解答;
(3)20℃时 A物质的溶解度为10g,即100g水最多能溶解10gA物质,据此分析;
(4)由溶解度曲线图可以看出,在30℃时ABC的溶解度关系为A>B>C,根据饱和溶液中溶质质量分数的计算公式
 ×100%,可以判断此时饱和溶液中质量分数关系为A>B>C,降温后A、B溶液中均有晶体析出,还是饱和溶液,但在10℃时,A的溶解度比B小,所以此时溶质质量分数为:B>A,C的溶解度随温度降低而升高变为不饱和溶液,则溶质质量分数将不变,最后进行综合比较得出答案.
×100%,可以判断此时饱和溶液中质量分数关系为A>B>C,降温后A、B溶液中均有晶体析出,还是饱和溶液,但在10℃时,A的溶解度比B小,所以此时溶质质量分数为:B>A,C的溶解度随温度降低而升高变为不饱和溶液,则溶质质量分数将不变,最后进行综合比较得出答案.解答:解:(1)由溶解度曲线图可以看出,在30℃时A、B、C三种物质的溶解度由小到大的顺序是C、B、A;
(2)A物质的溶解度受温度的影响较大,随温度的升高而增大,故可采用降温或加入溶质的方法使其变为饱和溶液;
(3)20℃时 A物质的溶解度为10g,即100g水最多能溶解10gA物质,所以将A物质40g加入到50g水中充分搅拌,可得50g水最多溶解5gB物质,所形成溶液的质量是55g;
(4)由溶解度曲线图可以看出,在30℃时ABC的溶解度关系为A>B>C,可以判断此时其质量分数关系为A>B>C,降温后A、B溶液中均有晶体析出,还是饱和溶液,但在10℃时,A的溶解度比B小,所以此时溶质质量分数为:B>A,C的溶解度随温度降低而升高变为不饱和溶液,则溶质质量分数将不变,故所得溶液的溶质质量分数由大到小的顺序是BAC;
故答案为:(1)C、B、A;(2)加入A物质或降低温度;(3)55;(4)B、A、C.
点评:本题主要考查了固体溶解度曲线所表示的意义,饱和溶液和不饱和溶液的相互转化等知识,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
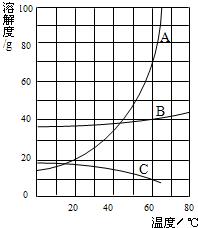 17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题.
17、如图是A、B、C三种固体物质的溶解度曲线示意图,试回答下列问题.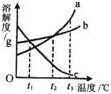 29、如图是a、b、c三种固体物质的溶解度曲线图.
29、如图是a、b、c三种固体物质的溶解度曲线图.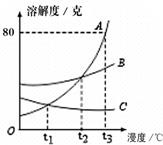 16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答:
16、如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答: (1)如图是A、B、C三种物质的溶解度曲线.请回答:
(1)如图是A、B、C三种物质的溶解度曲线.请回答: