题目内容
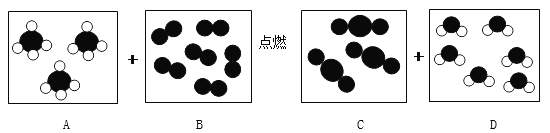
【题目】二氧化氯(ClO2)可用于自来水消毒,它具有显著的杀菌能力,制取ClO2的化学方程式为2X+4HCl=2 ClO2![]() +Cl2
+Cl2 ![]() +2NaCl+2H2O,则X的化学式为
+2NaCl+2H2O,则X的化学式为
A. NaClO3 B. NaClO C. HClO3 D. Na2CO3
【答案】A
【解析】
根据质量守恒定律:反应前后原子种类、原子数目均不变,由反应的化学方程式2X+4HCl=2 ClO2![]() +Cl2
+Cl2 ![]() +2NaCl+2H2O,反应前氯、氢原子个数分别为4、4,反应后的生成物中氯、钠、氧、氢原子个数分别为6、2、6、4,根据反应前后原子种类、数目不变,则2X分子中含有2个氯原子、6个氧原子、2个钠原子,则每个X分子由1个氯原子、3个氧原子、1个钠原子,则物质X的化学式为NaClO3,故选A。
+2NaCl+2H2O,反应前氯、氢原子个数分别为4、4,反应后的生成物中氯、钠、氧、氢原子个数分别为6、2、6、4,根据反应前后原子种类、数目不变,则2X分子中含有2个氯原子、6个氧原子、2个钠原子,则每个X分子由1个氯原子、3个氧原子、1个钠原子,则物质X的化学式为NaClO3,故选A。

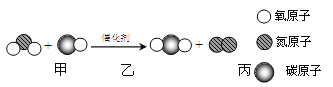
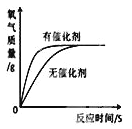
【题目】人教版新课标化学教材九年级上册(2012教育部审定)“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(实验探究)
实验步骤 | 实验现象 |
I.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
III.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
IV分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
(实验结论):(1)A中产生的气体是_________;
(2)实验II、III证明:氧化铁的__________在反应前后均没有发生变化。
(3)写出氧化铁催化过氧化氢分解的化学方程式___________。
(实验评价)实验设计IV的目的是____________;
(实验拓展)查阅资料得知,CuO、CuSO4、、、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是__________。
A、MnO2只能作过氧化氢溶液分解的催化剂
B、同一个化学反应可以有多种催化剂
C、催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他反应的反应物或生成物