题目内容
【题目】根据如图所示信息回答问题:

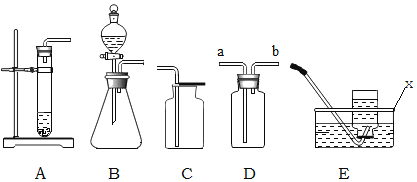
(1)根据图甲提供的内容。请你写出该元素的一条信息_____。
(2)图乙是某原子的结构示意图。x=_____,该元素属于_____(填“金属”或“非金属”)元素。
(3)图丙是钠原子的结构示意图,在化学反应中,该原子容易_____(填“得到”或“失去”)_____个电子形成钠离子。钠离子的符号是_____。
【答案】氯元素符号是Cl 7 非金属 失去 1 Na+
【解析】
在原子中,质子数等于核电荷数等于原子序数属于核外电子数,最外层电子数小于4反应中易失去电子。
(1)元素周期表中每一小方格中左上角数字表示原子序数即核电荷数,符号表示元素符号,下方数字表示相对原子质量。可查出关于氯元素的一条信息:氯元素符号是Cl等。
(2)当质子数=核外电子数,为原子,x=9-2=7.该元素的核内质子数为9,为氟元素,为非金属元素。
(3)钠原子中有11个质子,它属于金属元素,在化学反应中,钠原子最外层电子数是1,容易失去电子,所形成的粒子的符号是Na+。

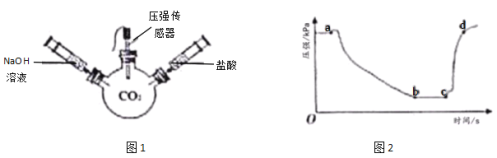
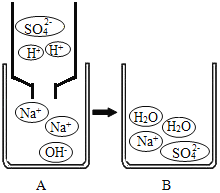
【题目】向一定量的NaOH溶液中慢慢通入CO2气体,看不到明显现象。某实验小组的同学对所得溶液成分进行了如下探究。请你参与他们的探究活动,并完成以下问题:
(提出问题)所得溶液中溶质的成分是什么?
(査阅资料)资料一:将CO2气体慢慢地通入一定量的NaOH溶液中,可能发生以下两个化学反应:
先发生反应:2NaOH+CO2═Na2CO3+H2O
当NaOH反应完全后,继续发生反应:Na2CO3+CO2+H2O═2NaHCO3
資料二;Ca(HCO3)2易溶于水;CaCl2溶液与NaCl溶液均呈中性; NaHCO3溶液呈碱性,可使酚酞溶液变红色。
(猜想与假设)小组同学通过讨论,提出了以下四种猜想
猜想一:溶质为NaOH和Na2CO3
猜想二:溶质全为Na2CO3
(1)你认为猜想三:溶质为_____
猜想四:溶质全为 NaHCO3
(实验探究)小组同学设计并完成了如下实验:
实验步骤 | 实验过程 | 实验现象 | 实验结论 |
① | 取适量反应后的溶液置于试管 中,加入过量CaCl2溶液 | 有白色沉淀生成 | (2)猜想_____不成立 |
② | 取适量步骤①反应后的上层清 液,滴加几滴酚酞溶液 | (3)现象为_____ | 猜想二不成立 |
③ | 取适量步骤①反应后的上层清 液,加入适量稀HCl | 有气泡产生 | (4)猜想_____成立 |
(实验总结)针对上述实验,实验小组的同学总结并写出了上述探究过程中的各步反应方程式。
(5)你认为步骤①发生反应的化学方程式是_____。