题目内容
 (2012?泉州模拟)在初三化学实验复习课上,老师提供了三瓶无色溶液,其中一瓶是稀盐酸,另外两瓶没有贴标签,分别是碳酸钠溶液和氢氧化钠溶液.
(2012?泉州模拟)在初三化学实验复习课上,老师提供了三瓶无色溶液,其中一瓶是稀盐酸,另外两瓶没有贴标签,分别是碳酸钠溶液和氢氧化钠溶液.复习内容一:鉴别两瓶没有贴标签无色溶液
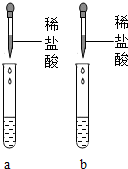
同学们设计了实验方案,分别取样于试管a、b两支试管中,再进行如图所示的实验操作.
(1)观察有1支试管中有
气泡
气泡
产生,证明该溶液是碳酸钠溶液.(2)写出试管a或b中发生反应的化学方程式:
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
(写一个即可).实验结束后,老师要求同学们把鉴别后所得的溶液倒入盛回收液的A烧杯或B烧杯中.复习内容二:探究回收液中,影响溶液酸碱性的溶质成分
(3)小明同学取少量A烧杯的回收液,滴入紫色石蕊试液,石蕊试液变红,从而证明A烧杯的回收液呈
酸
酸
性.根据实验结果,你认为A烧杯的回收液中必含有的溶质是HCl、NaCl
HCl、NaCl
.(4)小影同学用玻璃棒蘸取B烧杯中的回收液滴在 pH试纸上,测得pH=9,证明B烧杯中的回收液呈
碱
碱
性.根据实验结果,小影猜想B烧杯回收液中可能含有的溶质是:①氢氧化钠;②碳酸钠;③氢氧化钠和碳酸钠.【查阅资料】CaCl2溶液呈中性,可与碳酸钠溶液发生如下反应:Na2CO3+CaCl2=2NaCl+CaCO3↓
【查阅资料】
| 实验步骤 | 实验现象 | 实验结论 |
| Ⅰ.取少量B烧杯中的回收液于试管中,滴入饱和氢氧化钙溶液. | 产生白色沉淀 | B烧杯中的回收液中含有 碳酸钠 碳酸钠 |
| Ⅱ.①另取少量B烧杯中的回收液于试管中,滴入足量的 CaCl2 CaCl2 溶液.②过滤,往滤液中滴加 酚酞试液 酚酞试液 |
①产生白色沉淀. ② 酚酞变红色(或无变化) 酚酞变红色(或无变化) |
B烧杯中的回收液中 有氢氧化钠(或没有氢氧化钠) 有氢氧化钠(或没有氢氧化钠) |
③(或②)
③(或②)
是正确的.【能力提升】
(6)老师把A、B两烧杯中的回收液混合在一起,并测得混合液的pH=4,要求同学们选择下列其中一种试剂,通过加入过量的该试剂,以调节废液的pH=7,你认为他们应选择
C
C
(填标号).A.Ca(OH)2 B.CaO C.CaCO3 D.H2SO4.
分析:碳酸钠能与盐酸反应,生成氯化钠和水和二氧化碳,因此有气泡冒出;滴入紫色石蕊试液,石蕊试液变红,从而证明A烧杯的回收液呈酸性,因此溶液中有盐酸,还有新生成的氯化钠.测得pH=9,证明B烧杯中的回收液呈碱性;取少量B烧杯中的回收液于试管中,滴入饱和氢氧化钙溶液,碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,因此产生白色沉淀,烧杯中的回收液中含有碳酸钠;另取少量B烧杯中的回收液于试管中,滴入足量的CaCl2溶液,过滤,往滤液中滴加酚酞试液,酚酞变红色(或无变化),有氢氧化钠(或没有氢氧化钠),因此小影同学的猜想③(或②)是正确的.pH=4溶液呈酸性,应该选用碳酸钙以调节废液的pH=7,因为氢氧化钙和生石灰过量会大于7.
解答:解:(1)碳酸钠能与盐酸反应,生成氯化钠和水和二氧化碳,因此有气泡冒出故答案为:气泡
(2)碳酸钠能与盐酸反应,生成氯化钠和水和二氧化碳,配平即可,故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑
(3)滴入紫色石蕊试液,石蕊试液变红,从而证明A烧杯的回收液呈酸性,因此溶液中有盐酸,还有新生成的氯化钠;故答案为:酸;HCl、NaCl
(4)测得pH=9,证明B烧杯中的回收液呈碱性;故答案为:碱
(5)取少量B烧杯中的回收液于试管中,滴入饱和氢氧化钙溶液,碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,因此产生白色沉淀,烧杯中的回收液中含有碳酸钠;另取少量B烧杯中的回收液于试管中,滴入足量的CaCl2溶液,过滤,往滤液中滴加酚酞试液,酚酞变红色(或无变化),有氢氧化钠(或没有氢氧化钠),因此小影同学的猜想③(或②)是正确的.故答案为:Ⅰ.碳酸钠;①CaCl2;②酚酞试液;酚酞变红色(或无变化);有氢氧化钠(或没有氢氧化钠);③(或②)
(6)pH=4溶液呈酸性,应该选用碳酸钙以调节废液的pH=7,因为氢氧化钙和生石灰过量会大于7.故答案为:C
(2)碳酸钠能与盐酸反应,生成氯化钠和水和二氧化碳,配平即可,故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑
(3)滴入紫色石蕊试液,石蕊试液变红,从而证明A烧杯的回收液呈酸性,因此溶液中有盐酸,还有新生成的氯化钠;故答案为:酸;HCl、NaCl
(4)测得pH=9,证明B烧杯中的回收液呈碱性;故答案为:碱
(5)取少量B烧杯中的回收液于试管中,滴入饱和氢氧化钙溶液,碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,因此产生白色沉淀,烧杯中的回收液中含有碳酸钠;另取少量B烧杯中的回收液于试管中,滴入足量的CaCl2溶液,过滤,往滤液中滴加酚酞试液,酚酞变红色(或无变化),有氢氧化钠(或没有氢氧化钠),因此小影同学的猜想③(或②)是正确的.故答案为:Ⅰ.碳酸钠;①CaCl2;②酚酞试液;酚酞变红色(或无变化);有氢氧化钠(或没有氢氧化钠);③(或②)
(6)pH=4溶液呈酸性,应该选用碳酸钙以调节废液的pH=7,因为氢氧化钙和生石灰过量会大于7.故答案为:C
点评:本考点考查的是酸碱盐的性质和中和反应的应用,酸碱盐是初中阶段的一个重点,也是一个难点.掌握好酸碱盐的性质,并理解应用,中和反应的应用也就会迎刃而解.本考点主要出现在实验题中.

练习册系列答案
相关题目

