��Ŀ����
����Ŀ���±���Ca��OH��2��NaOH���ܽ�����ݣ���ش��������⣺
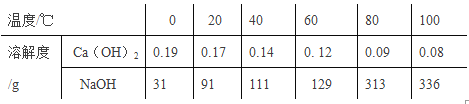
��1�������ϱ����ݣ�����Ca��OH��2��NaOH���ܽ�����ߣ���ͼ��ʾ�ܱ�ʾNaOH�ܽ�����ߵ��� ����A��B��

��2��Ҫ���һƿ�ӽ����͵�Ca��OH��2��Һ��ɱ�����Һ�������ʩ�У��ټ����������ƣ��������¶ȣ��۽����¶ȣ��ܼ���ˮ��������ˮ���ٻָ���ԭ�¶ȣ�������ʯ�ң����д�ʩ��ȷ���� ��
A���ڢܢ� B���ۢ� C���٢ۢݢ� D���٢ڢݢ�
��3��20��ʱ��191g����NaOH��Һ������10gˮ���ٽ��µ�20����������NaOH���������Ϊ ��
��4������60��ʱ��Ca��OH��2��NaOH�������ʵı�����Һ����Ҫ�õ��ϴ�����NaOH���壬Ӧ��ȡ������������ ��
���𰸡���1��A��2��D��3��9.1g��4�����½ᾧ�ٹ���
��������
�����������1���ɱ������ܽ�����ݿ�֪�������Ƶ��ܽ�����¶ȵ����߶������������Ƶ��ܽ�����¶ȵ����߶���С����A��ʾ�����������Ƶ��ܽ�����ߣ�B��ʾ�����������Ƶ��ܽ�����ߣ�
��2��Ҫ��һƿ�ӽ����͵�Ca��OH��2��Һ��ɱ�����Һ�������У������ʡ����������ܼ������¡���ѡD��
��3��20��ʱ���������Ƶ��ܽ��Ϊ91g����100gˮ�����ܽ�91g�������Ƶõ�����״̬����20��ʱ��191g����NaOH��Һ�����ʵ�����Ϊ91g���ܼ�������Ϊ100g������10gˮ���ٽ��µ�20�棬�ܽ�Ȳ��䣬�ܼ���������Ϊ90g���ʻ�����9.1g�������ƣ�
��5���������Ƶ��ܽ����¶ȵ�Ӱ��仯�ϴʿɲ��ý��½ᾧ�ķ����ᴿ�����Ƚ��º���˼��ɵõ��ϴ������������ơ�









