题目内容
【题目】有一包固体粉末A,可能含有Mg、Al2O3、CuO、NaCl、Na2CO3、NaOH中的一种或几种,为探究其成分,甲同学取少量的A做如下实验,现象如图所示。
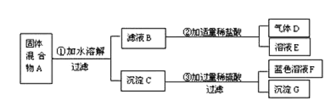
根据实验过程中的现象判断:
(1)写出生成沉淀G的化学方程式是_____________________________。
(2)混合物A中一定有________________。
(3)溶液F中,一定存在溶质是___________________________。
(4)滤液B中,可能存在的溶质是______________,若要证明该物质是否存在,应补做实验是(写出主要实验步骤、现象及结论,如有多种任选一种即可)________________________________________________________________________。
【答案】Mg+CuSO4=MgSO4+Cu Na2CO3、Mg、CuO MgSO4、CuSO4、H2SO4 NaCl、NaOH 取滤液B少量,先加足量稀硝酸,再滴加硝酸银溶液,如产生白色沉淀,则有NaCl或取滤液B少量,先加足量氯化钙溶液,静置后滴加无色酚酞溶液,如变红,则有NaOH
【解析】
沉淀C加入稀硫酸后有蓝色溶液F生成,故沉淀C中一定含有氧化铜固体,有沉淀G生成,说明原物质中一定有镁,镁与生成的硫酸铜反应生成了铜。滤液中加入稀盐酸有气体生成,说明原物质中一定有碳酸钠。
(1)由分析可知,生成沉淀G的方程式为:Mg+CuSO4=MgSO4+Cu。
(2)由分析可知,原混合物中一定含有Na2CO3、Mg、CuO。
(3)蓝色溶液中一定含有硫酸铜,由于有沉淀铜生成,故溶液中也一定含有生成的硫酸镁和过量的稀硫酸。
(4)滤液B中一定含有碳酸钠,可能含有氯化钠和氢氧化钠。

【题目】已知M、N分别是稀硫酸、氢氧化钠溶液中的一种。某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH,如下图所示:
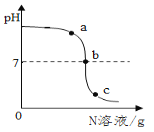
(1)M是__。
(2)反应过程中,老师分别取图中a、b、c三处所对应的溶液,打乱顺序后,请同学们用最简便的方法将三种溶液鉴别的方法是__,
小明和小红采用了另外一种实验方案,分别取其中一种溶液进行实验:小明向所取溶液中加入__溶液,观察到有蓝色沉淀生成。
结论:是a处溶液。
小红向少量另一种溶液中滴加酚酞溶液,观察到___。
结论:是b处或c处溶液。
为进一步确定该溶液成分,小红又设计并完成如下实验:
实验步骤 | 实验现象 | 结论及化学方程式 |
取少量氧化铁,加入足量该溶液 | 固体完全溶解,且___ | 相关的化学方程式为__。为c处溶液,并推知c处溶液中含有的离子有___(填写离子符号) |
结论:剩余一种为b处溶液。