题目内容
某同学用铁、氧化铜、稀硫酸为原料,设计了两个实验室制取铜的方案.
方案一:CuO
CuSO4
Cu
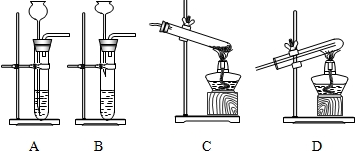
方案二:Fe
H2
Cu
(1)进行第一个方案的过程有蓝色溶液产生,写出实验该方案所发生反应的方程式:
______;______.
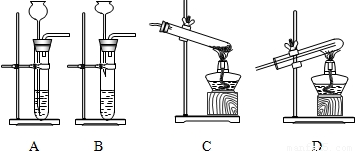
(2)进行第二个方案需用到下列装置中的______(填序号).用该方案制得的铜中可能混有的杂质是______.
(3)两个实验方案中第______方案更好,理由是(只要求写三种):
①______.
②______.
③______.
方案一:CuO
| H2SO4 |
| Fe |
方案二:Fe
| H2SO4 |
| CuO |
(1)进行第一个方案的过程有蓝色溶液产生,写出实验该方案所发生反应的方程式:
______;______.
(2)进行第二个方案需用到下列装置中的______(填序号).用该方案制得的铜中可能混有的杂质是______.

(3)两个实验方案中第______方案更好,理由是(只要求写三种):
①______.
②______.
③______.
(1)第一个方案的过程有蓝色溶液产生,说明生成了硫酸铜,氧化铜和硫酸反应生成蓝色的硫酸铜和水,铁和硫酸铜反应生成硫酸亚铁和铜,
故答案为:CuO+H2SO4=CuSO4+H2O Fe+CuSO4=FeSO4+Cu;
(2)铁和硫酸反应生成硫酸亚铁和氢气,再利用氢气的还原性,和氧化铜反应在加热的条件下生成铜和水,故答案为:A、D 氧化铜;
(3)第一个方案不用加热,常温就可以进行,第二个方案中有氢气参加反应,需要检验氢气纯度,故答案为:第一个,①安全②操作简单③常温下就能反应.
故答案为:CuO+H2SO4=CuSO4+H2O Fe+CuSO4=FeSO4+Cu;
(2)铁和硫酸反应生成硫酸亚铁和氢气,再利用氢气的还原性,和氧化铜反应在加热的条件下生成铜和水,故答案为:A、D 氧化铜;
(3)第一个方案不用加热,常温就可以进行,第二个方案中有氢气参加反应,需要检验氢气纯度,故答案为:第一个,①安全②操作简单③常温下就能反应.

练习册系列答案
相关题目

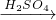 CuSO4
CuSO4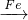 Cu
Cu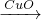 Cu
Cu
 CuSO4
CuSO4 Cu
Cu H2
H2 Cu
Cu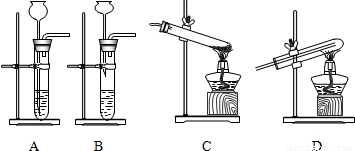
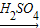 CuSO4
CuSO4 Cu
Cu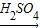 H2
H2 Cu
Cu