题目内容
【题目】水和空气都是我们赖以生存的重要物质。请用所学知识回答下列问题:
(1)我们饮用的自来水属于_____(填“纯净物”或“混合物”),在自来水净化过程中加入活性炭的作用是_____。
(2)水沸腾时没有发生变化的是_____(填序号)。
A 分子间的间隔 B 分子的大小 C 分子的种类
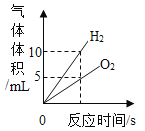
(3)电解水的过程中电源正极和负极产生气体体积比是_____。
(4)未经脱硫处理的煤燃烧会排放出形成酸雨的_____(填名称)气体。
(5)乙醇作为一种可再生能源被广泛关注,请写出乙醇燃烧的化学方程式_____。
【答案】混合物 吸附色素和异味(或吸附作用) BC 1:2 二氧化硫 C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
【解析】
电解水正极生成氧气,负极生成氧气,二氧化硫和水反应生成亚硫酸,乙醇在氧气中燃烧生成二氧化碳和水。
(1)我们饮用的自来水含有较多可溶性杂质,属于混合物,活性炭具有吸附性,在自来水净化过程中加入活性炭的作用是吸附色素和异味(或吸附作用)。
(2)水沸腾时分子间的间隔变大,没有发生变化的是分子的大小、分子的种类,故选BC。
(3)电解水正极生成氧气,负极生成氧气,故电解水的过程中电源正极和负极产生气体体积比是1:2。
(4)硫燃烧生成二氧化硫,未经脱硫处理的煤燃烧会排放出形成酸雨的二氧化硫气体。
(5)乙醇在氧气中燃烧生成二氧化碳和水,反应的化学方程式为C2H5OH+3O2![]() 2CO2+3H2O。
2CO2+3H2O。

【题目】两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.
(提出问题)这两瓶黑色粉末A和B分别是什么物质?
(猜想1)甲同学:A是铁粉,B是二氧化锰.
乙同学:A是炭粉,B是氧化铜.
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
①取少量A粉末于试管中,加入适量稀硫酸. | 黑色粉末不溶解,没有气体产生. | A粉末一定不是_____. |
②取少量B粉末于试管中,加入适量稀硫酸. | _____. | B粉末是氧化铜. |
(反思与拓展)
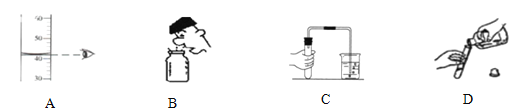
(1)将这两种黑色粉末混合加热(如图),观察到黑色粉末逐渐变为红色,澄清石灰水变浑浊.黑色粉末A和B发生反应的化学方程式为_____.实验结束时,先将导管移出,再熄灭酒精灯的原因是_____.
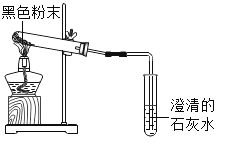
(2)乙同学的猜想正确.