题目内容
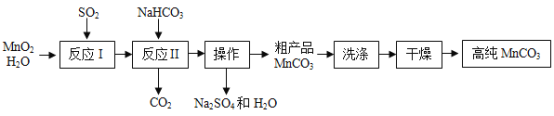
【题目】实验室以MnO2为原料制备少量高纯MnCO3的流程如下:
已知:①反应Ⅰ的化学方程式:![]() ;②MnCO3、Mn(OH)2 均难溶于水,MnCO3在100℃时开始分解。
;②MnCO3、Mn(OH)2 均难溶于水,MnCO3在100℃时开始分解。
(1)反应Ⅰ属于基本反应类型中的_____________反应。
(2)流程中“操作”的名称为_____________,所需要的主要玻璃仪器有玻璃棒、烧杯、_____________。
(3)反应Ⅱ的化学方程式为_____________,反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有_______________(填化学式)。
(4)验证MnCO3粗产品表面附着有Na2SO4杂质:取样品少许,向其中加入水,搅拌、过滤,向滤液中加入适量的____________(填化学式)溶液,有白色沉淀产生。
(5)为获得高纯MnCO3,需选择“低温”干燥的原因是__________________。
【答案】化合 过滤 漏斗 ![]() Mn(OH)2 BaCl2 MnCO3在100°C以上会分解
Mn(OH)2 BaCl2 MnCO3在100°C以上会分解
【解析】
(1)化合反应是指由两种或两种以上物质生成另一种物质的反应。由题意可知,反应I的化学方程式:![]() ,为两种物质变成一种, 多变一,为化合反应,所以反应I属于基本反应类型中的化合反应;
,为两种物质变成一种, 多变一,为化合反应,所以反应I属于基本反应类型中的化合反应;
(2)流程中“操作”是将难溶性物质碳酸锰和硫酸钠溶液分离的,为过滤,所需要的主要玻璃仪器有漏斗、玻璃棒、烧杯;
(3)反应Ⅱ中加入的是反应I的生成物硫酸锰和新加入的碳酸氢钠,生成物为过滤得到的碳酸锰和溶液中的硫酸钠以及生成的气体二氧化碳。对应的化学方程式为: ![]() 。反应II需控制溶液的酸碱性,若碱性过强,则硫酸锰和碱反应生成难溶性氢氧化锰沉淀,对应的化学式为Mn(OH)2;
。反应II需控制溶液的酸碱性,若碱性过强,则硫酸锰和碱反应生成难溶性氢氧化锰沉淀,对应的化学式为Mn(OH)2;
(4)验证MnCO3粗产品表面附着有Na2SO4杂质,也就是检验硫酸根的存在:取样品少许,向其中加入水,搅拌、过滤,向滤液中加入适量的BaCl2溶液,有白色沉淀产生;
(5)为获得高纯MnCO3,需选择“低温”干燥的原因是MnCO3的分解温度为100℃,为防止MnCO3高温分解,影响高纯MnCO3的纯度。

【题目】下列物质中的杂质![]() 括号内是杂质
括号内是杂质![]() ,下列操作方法正确的是( )
,下列操作方法正确的是( )
选项 | 物质 | 操作方法 |
A | CO2(CO) | 点燃 |
B | CaO | 加足量的水,充分搅拌后过滤 |
C | NaOH溶液 | 通入过量 |
D | Fe(Fe2O3) | 高温条件下通入足量的CO |
A.AB.BC.CD.D