题目内容
【题目】已知一定质量的纯净物A跟16g氧气进行充分的燃烧,恰好完全反应后,生成11g二氧化碳和9g水,请回答以下问题:
(1)参加反应的物质A的质量是_____;
(2)组成物质A的元素,一定有_____(填元素符号)
(3)物质A中各元素的质量比是多少?_____(写计算过程)
【答案】4g 碳、氢 3:1
【解析】
(1)根据质量守恒定律参加反应的物质A的质量为11g+9g-16g=4g;
(2)11g二氧化碳中碳元素的质量=11g×![]() =3g;9g水中氢元素的质量=9g×
=3g;9g水中氢元素的质量=9g×![]() =1g;3g+1g=4g,因此根据质量守恒定律可知,该物质中不含有氧元素;
=1g;3g+1g=4g,因此根据质量守恒定律可知,该物质中不含有氧元素;
(3)物质A中碳、氢元素的质量比为3g:1g=3:1;
故答案为:(1)4g;(2)碳、氢;(3)3:1.

【题目】催化剂在化学反应中起着非常重要的作用,某兴趣小组进行如下探究。
探究一 催化剂的选择
研究表明,许多金属氧化物对氯酸钾有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
温度 | Fe2O3 | Al2O3 | CuO | MgO |
开始反应 | 470 | 515 | 305 | 490 |
剧烈反应 | 490 | 540 | 350 | 545 |
(1)上述实验中,从温度对反应催化效果来看,最好选用__________作催化剂。
探究二 氧化铜与二氧化锰的催化效果进行比较
用如图装置进行实验,实验均以生成25mL气体为准,可能影响实验的因素均已忽略,相关装置和数据见下表:
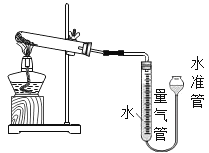
序号 | KClO3质量 | 催化剂质量 | 待测试剂 |
① | 2.45g | — | a |
② | 2.45g | 0.51gMnO2 | b |
③ | 2.45g | 0.51gCuO | c |
(2)上述实验中的“待测数据”是________________。若b_________c(填“>”、“=”或“<”)可知在某温度下氧化铜对氯酸钾分解效果更好。
探究三 氧化铜与二氧化锰的对于过氧化氢的催化效果进行比较
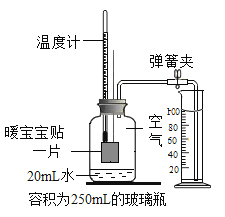
安妮同学用如图1所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,分别将注射器内盛有的双氧水注入试管中,利用注射器收集氧气,收集到氧气的体积和时间的关系如图2所示。
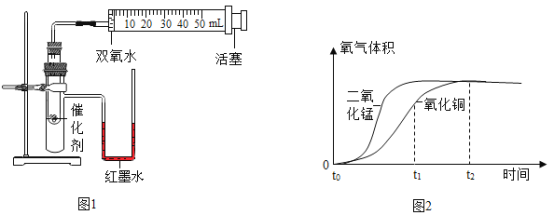
(3)装入药品前检查该装置气密性的方法是_____________,开始实验时注入双氧水的方法是________(填序号),另一种方法除了误差较大,还可能造成的后果是_____________。
A快速推注射器活塞 B缓慢推注射器活塞
(4)实验中造成U形管内红墨水液面左低右高的可能原因是_____________。
(5)通过图象2除了能得出二氧化锰催化效果比氧化铜好,还能得出的结论是________________。
(6)由氧化铜催化的反应,t1-t2时间段反应速率逐渐变_______(填“快”或“慢”),原因是___________________。
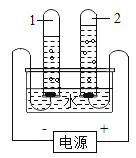
【题目】水在化学实验中有多种用途,对下列实验中水的作用解释不正确的是( )
A | B | C | D | |
实 验 装 置 |
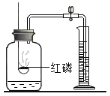
硫在氧气中燃烧 |
测定空气中氧气含量 |
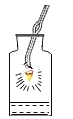
铁丝在氧气中燃烧 |
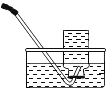
排水法收集氧气 |
作用 | 集气瓶中的水; 吸收热量,防止集气瓶炸裂。 | 量筒中的水: 通过体积变化得出 空气中氧气的体积 | 集气瓶中的水: 冷却溅落熔融物, 防止集气瓶炸裂 | 集气瓶中先装满的水:先排尽瓶中空气并便于观察氧气何时集满。 |
A.AB.BC.CD.D
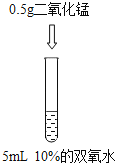
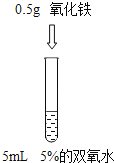
【题目】为了探究”影响双氧水制氧气的速率”的因素,某学习小组设计了下列实验,下列说法正确的是( )
实验① | 实验② | 实验③ |
|
|
|
A. 对比实验②和③,可研究双氧水的质量分数对反应速率的影响
B. 对比实验①和②,可研究双氧水的质量分数对反应速率的影响
C. 对比实验②和③,可研究催化剂的种类对反应速率的影响
D. 对比实验①和②,可研究催化剂的种类对反应速率的影响