题目内容
 如图是甲、乙两种固体物质的溶解度曲线图
如图是甲、乙两种固体物质的溶解度曲线图(1)将t1℃时甲、乙的饱和溶液同时升温至t2℃所得溶液中溶质的质量分数的大小关系为
甲=乙
甲=乙
(不考虑水的蒸发)(2)t2℃时,将等质量的甲、乙两种物质加水溶解配成饱和溶液,所得溶液质量的大小关系为
甲<乙
甲<乙
(3)t2℃时,将50g甲放入50g水中充分搅拌后所得溶液中溶质的质量分数为
37.5%
37.5%
.分析:(1)据物质的溶解度随温度的变化及溶质的质量分数分析判断;
(2)据该温度下物质的溶解度大小分析解答;
(3)据溶质的质量分数计算方法分析解答.
(2)据该温度下物质的溶解度大小分析解答;
(3)据溶质的质量分数计算方法分析解答.
解答:解:(1)AB的溶解度随温度的升高而增大,据饱和时质量分数的计算式
×100%可知:溶解度相等则溶质的质量分数相等,t1℃时AB的溶解度相等,所以A、B两种物质的饱和溶液溶质的质量分数A=B;将t1℃的A、B两种物质的饱和溶液升温到t2℃时,其溶液中溶质、溶剂的质量不变,故所得溶液中溶质质量分数的关系为A=B;
(2)t2℃时甲的溶解度大于乙的溶解度,所以将等质量的甲、乙两种物质加水溶解配成饱和溶液,乙需要的水多,则所得溶液质量的大小关系为甲小于乙;
(3)t2℃时甲的溶解度是60g,所以将50g甲放入50g水中充分搅拌后最多溶解30g,所得溶液中溶质的质量分数为
×100%=37.5%;
故答案为:(1)甲=乙;(2)甲<乙;(3)37.5%.
| 溶解度 |
| 溶解度+100g |
(2)t2℃时甲的溶解度大于乙的溶解度,所以将等质量的甲、乙两种物质加水溶解配成饱和溶液,乙需要的水多,则所得溶液质量的大小关系为甲小于乙;
(3)t2℃时甲的溶解度是60g,所以将50g甲放入50g水中充分搅拌后最多溶解30g,所得溶液中溶质的质量分数为
| 30g |
| 80g |
故答案为:(1)甲=乙;(2)甲<乙;(3)37.5%.
点评:本题考查了溶解度曲线的应用,解答时要在掌握溶解度的概念、饱和溶液中溶质质量分数的计算方法的基础上分析解答,能较好考查学生分析解决问题的能力.

练习册系列答案
相关题目
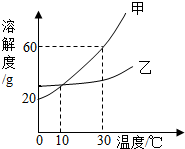 (2013?江都市模拟)如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )
(2013?江都市模拟)如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )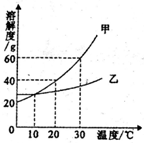 如图是甲、乙两种固体物质的溶解度曲线,下列叙述中正确是( )
如图是甲、乙两种固体物质的溶解度曲线,下列叙述中正确是( )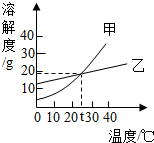 (2012?平顶山一模)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
(2012?平顶山一模)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )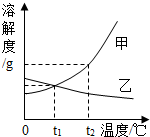 (2013?市中区一模)水是生命之源,生产之要,生活之基.泉城市民更要珍惜水、节约水、保护水.请完成下列问题:
(2013?市中区一模)水是生命之源,生产之要,生活之基.泉城市民更要珍惜水、节约水、保护水.请完成下列问题: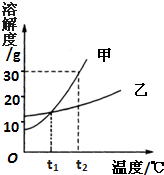 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.