题目内容
(2分)某地一不法商贩销售的含NH4HCO3的氮肥,经检验含氮的质量分数为14%。
(1)NH4HCO3中碳、氢元素质量比为________。
(2)该商贩所售每袋50 kg氮肥中,实验含NH4HCO3________kg。(结果精确到0.1 kg)
(1)NH4HCO3中碳、氢元素质量比为________。
(2)该商贩所售每袋50 kg氮肥中,实验含NH4HCO3________kg。(结果精确到0.1 kg)
(2分)(1)12∶5 (2)39.5
分析:(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比即可求得NH4HCO3中碳、氢元素质量;
(2)利用不法商贩销售的NH4HCO3氮肥中检验出的氮的质量分数为14%,计算每袋该氮肥(50kg)中氮元素的质量,然后利用NH4HCO3中氮元素的质量分数,计算实际含NH4HCO3的质量.
解:(1)碳酸氢铵的化学式为NH4HCO3;根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;
则NH4HCO3中碳、氢元素质量比为12:(1×5)=12:5;
(2)NH4HCO3中氮元素的质量分数为: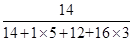 ×100%=17.7%
×100%=17.7%
50kg氮肥中实际含N元素的质量为50kg×14%=7kg;
则50kg氮肥中实际含NH4HCO3的质量为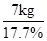 =39.5kg;
=39.5kg;
故答案为:(1)12:5 (2)39.5.
点评:根据一定量化合物中某组成元素的质量=化合物的质量×化合物中该元素的质量分数,已知组成元素的质量及质量分数,可计算化合物的质量.
(2)利用不法商贩销售的NH4HCO3氮肥中检验出的氮的质量分数为14%,计算每袋该氮肥(50kg)中氮元素的质量,然后利用NH4HCO3中氮元素的质量分数,计算实际含NH4HCO3的质量.
解:(1)碳酸氢铵的化学式为NH4HCO3;根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;
则NH4HCO3中碳、氢元素质量比为12:(1×5)=12:5;
(2)NH4HCO3中氮元素的质量分数为:
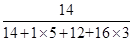 ×100%=17.7%
×100%=17.7%50kg氮肥中实际含N元素的质量为50kg×14%=7kg;
则50kg氮肥中实际含NH4HCO3的质量为
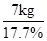 =39.5kg;
=39.5kg;故答案为:(1)12:5 (2)39.5.
点评:根据一定量化合物中某组成元素的质量=化合物的质量×化合物中该元素的质量分数,已知组成元素的质量及质量分数,可计算化合物的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目