题目内容
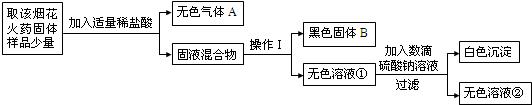
19、某固体样品中,可能含有Na2CO3、Na2SO4、NaCl、Cu(NO3)2、Ca(NO3)2中的一种或几种.将样品溶于水得到无色溶液,滴加BaCl2溶液后产生白色沉淀.过滤,向白色沉淀中加入足量的稀硝酸,沉淀全部溶解.推断:该固体中肯定存在
Na2CO3
,肯定不存在Na2SO4、Cu(NO3)2、Ca(NO3)2
.分析:根据题意进行分析可知,沉淀全部溶解,沉淀不能有氯化银和硫酸钡,溶液无色,不能有带色的离子,结合题意再进行进一步的推导即可求得.
解答:解:样品溶于水,溶液为无色,溶液中没有硝酸铜,加氯化钡会生成白色沉淀,溶液中可能有碳酸钠和硫酸钠,但是生成的白色沉淀会全部溶于硝酸,所以一定有碳酸钠,一定没有硫酸钠,样品溶于水是无色,就一定没有氯化钙,故答案为:Na2CO3,Na2SO4、Cu(NO3)2、Ca(NO3)2,
点评:本题主要对离子的共存问题进行了综合考察,在考虑问题是注意要全面.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
己知铁的氧化物有FeO、Fe2O3、Fe3O4,某固体样品由铁和氧两种元素组成,样品中铁与氧元素的质量比为
21:8,则下列关于该样品的组成的叙述中正确的是( )
21:8,则下列关于该样品的组成的叙述中正确的是( )
| A、该样品成分中一定含有Fe3O4 | B、若该样品含多种物质,则样品中一定含FeO | C、若该样品含多种物质,则样品中一定含Fe2O3 | D、该样品成分中不可能含有单质铁 |