题目内容
合理使用化肥可以提高农产品的产量和质量.某化肥溶液中含有溶质的质量分数为8%的KN03.
(1)KN03属于 (选填“氮肥”、“钾肥”或“复合肥料”).
(2)如果用溶质质量分数为20%的KN03溶液配制100g上述营养液,需溶质质量分数为20%的KN03溶液 g,加水 g.
(1)KN03属于
(2)如果用溶质质量分数为20%的KN03溶液配制100g上述营养液,需溶质质量分数为20%的KN03溶液
考点:常见化肥的种类和作用,用水稀释改变浓度的方法
专题:溶液的组成及溶质质量分数的计算,常见的盐 化学肥料
分析:(1)从KN03中含有氮元素和钾元素两种营养元素去分析解答;
(2)根据稀释前后溶质量的质量不变;溶质的质量分数=
×100%,可得溶质量的质量=溶液质量×溶质的质量分数去分析解答.
(2)根据稀释前后溶质量的质量不变;溶质的质量分数=
| 溶质的质量 |
| 溶液的质量 |
解答:解:(1)由于KN03中含有氮元素和钾元素两种营养元素,所以属于复合肥料;故答案为:复合肥料;
(2)根据稀释前后溶质量的质量不变;溶质的质量分数=
×100%,可得溶质量的质量=溶液质量×溶质的质量分数;
设20%的KN03溶液的质量为x,
x×20%=100g×8%
解之得:
x=40g
加水的质量为:100g-40g=60g;
故答案为:40 60.
(2)根据稀释前后溶质量的质量不变;溶质的质量分数=
| 溶质的质量 |
| 溶液的质量 |
设20%的KN03溶液的质量为x,
x×20%=100g×8%
解之得:
x=40g
加水的质量为:100g-40g=60g;
故答案为:40 60.
点评:稀释原则:稀释前后溶质量的质量不变.注意是质量不变不是体积不变.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
雅安地震发生后,为确保大灾之后无大疫,灾区使用了大量的消毒剂ClO2.工业上制取ClO2的原理之一是:2NaClO3+4X═2NaCl+2ClO2+Cl2↑+2H2O.下列有关说法正确的是( )
| A、上述反应属于分解反应 |
| B、ClO2中氯元素和氧元素的质量比为1:2 |
| C、X的化学式为HCl |
| D、上述反应的生成物都是由分子构成的 |
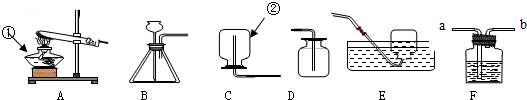
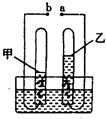 如图是通电分解水的简易装置图,回答下列问题.
如图是通电分解水的简易装置图,回答下列问题.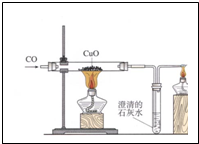 某兴趣小组利用如图装置进行试验,请回答相关的问题:
某兴趣小组利用如图装置进行试验,请回答相关的问题:
 如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法正确的是
如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法正确的是