题目内容
 (2010?常德)在校园文艺节上,萌萌同学表演的“水能生火“的化学小魔术博得了满堂彩,她向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.事后她对这魔术的化学原理很感兴趣,于是便和同学们一起探究起来.
(2010?常德)在校园文艺节上,萌萌同学表演的“水能生火“的化学小魔术博得了满堂彩,她向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.事后她对这魔术的化学原理很感兴趣,于是便和同学们一起探究起来.【提出问题】①过氧化钠和水反应生成了什么物质?
②脱脂棉为什么会燃烧?
【大胆猜想】①可能生成了一种气体和另一种物质.
②反应过程可能有能量变化.
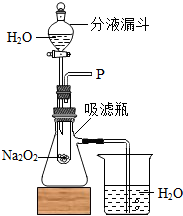
【设计装置】萌萌他们组装了如右图的装置进行实验.其中分液漏斗可通过活塞控制液流速度,吸滤瓶右侧有支管可导出气体(瓶内为空气).
【实验探究】探究l:反应生成的气体物质是什么?
探究2:脱脂棉为什么会燃烧?
(1)打开分液漏斗活塞,以适当的速度将水滴入Na2O2中,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明反应生成的气体是
氧气(或O2)
氧气(或O2)
.(2)实验中还观察到与吸滤瓶连接的导管在盛水的烧杯中有气泡冒出,试解释产生该现象的原因
Na2O2与水反应时,产生大量的热,吸滤瓶中空气受热膨胀产生气泡
Na2O2与水反应时,产生大量的热,吸滤瓶中空气受热膨胀产生气泡
,这一现象为
脱脂棉燃烧
脱脂棉燃烧
找到了依据.探究3:反应生成的另一种产物是什么?
(1)同伴强强猜想另一种物质是Na2CO3,萌萌认为不可能,萌萌的依据是
反应物中不含碳元素,根据质量守恒定律判断不可能生成碳酸钠
反应物中不含碳元素,根据质量守恒定律判断不可能生成碳酸钠
.如果你同意萌萌的意见,请你完成下表:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量探究1反应后的溶 液于试管中,加入稀盐酸. |
无现象 无现象 |
生成物中 生成物中 |
碱
碱
性,则这种产物应该为(写化学式)NaOH
NaOH
.【作出结论】由实验探究的结果,萌萌他们得出过氧化钠与水反应的化学方程式是
2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2H2O═4NaOH+O2↑
.分析:探究2:
(1)根据用带火星的木条靠近P处,木条复燃来确定气体;
(2)根据与吸滤瓶连接的导管在盛水的烧杯中有气泡冒出来分析锥形瓶内气体体积变化的原因;
探究3:
(1)根据反应物,利用元素守恒来分析反应产物;再利用生成物与盐酸反应,观察是否有气泡冒出来说明是否有碳酸钠生成;
(2)根据滴入无色酚酞试液变红色来确定溶液的酸碱性,利用元素守恒及溶液的酸碱性来推断反应产物;
【作出结论】利用反应物与生成物来书写反应的化学反应方程式.
(1)根据用带火星的木条靠近P处,木条复燃来确定气体;
(2)根据与吸滤瓶连接的导管在盛水的烧杯中有气泡冒出来分析锥形瓶内气体体积变化的原因;
探究3:
(1)根据反应物,利用元素守恒来分析反应产物;再利用生成物与盐酸反应,观察是否有气泡冒出来说明是否有碳酸钠生成;
(2)根据滴入无色酚酞试液变红色来确定溶液的酸碱性,利用元素守恒及溶液的酸碱性来推断反应产物;
【作出结论】利用反应物与生成物来书写反应的化学反应方程式.
解答:解:探究2(1)由氧气具有助燃性,且用带火星的木条靠近P处,木条复燃,说明该反应中有氧气生成,
故答案为:氧气(或O2);
(2)观察到与吸滤瓶连接的导管在盛水的烧杯中有气泡冒出,说明锥形瓶内的气体体积膨胀,则该反应发生时放出了大量的热,且脱脂棉燃烧
时温度应达到着火点,即当Na2O2与水反应时,产生大量的热且生成氧气使脱脂棉燃烧,
故答案为:Na2O2与水反应时,产生大量的热,吸滤瓶中空气受热膨胀产生气泡;脱脂棉燃烧;
探究3(1)因反应物为Na2O2和水,不含有碳元素,根据质量守恒定律可知,元素守恒说明生成物中不会有碳元素,则不可能生成碳酸钠,
利用盐酸来确定是否有碳酸钠生成,该实验设计如下,
实验步骤为:取少量探究1反应后的溶液于试管中,加入稀盐酸,
实验现象为:无现象,
实验结论为:生成物中无碳酸钠,
故答案为:反应物中不含碳元素,根据质量守恒定律判断不可能生成碳酸钠;
(2)由探究l反应后的溶液于试管中,滴入无色酚酞试液变红色,说明溶液显碱性,再根据反应物为Na2O2和水,由元素守恒,溶液中存在钠离子和氢氧根离子,即
该反应中的另一生成物因为NaOH,故答案为:碱;NaOH;
[作出结论]因该反应的反应物为Na2O2和水,生成物为NaOH和O2,则该反应为2Na2O2+2H2O═4NaOH+O2↑,故答案为:2Na2O2+2H2O═4NaOH+O2↑.
故答案为:氧气(或O2);
(2)观察到与吸滤瓶连接的导管在盛水的烧杯中有气泡冒出,说明锥形瓶内的气体体积膨胀,则该反应发生时放出了大量的热,且脱脂棉燃烧
时温度应达到着火点,即当Na2O2与水反应时,产生大量的热且生成氧气使脱脂棉燃烧,
故答案为:Na2O2与水反应时,产生大量的热,吸滤瓶中空气受热膨胀产生气泡;脱脂棉燃烧;
探究3(1)因反应物为Na2O2和水,不含有碳元素,根据质量守恒定律可知,元素守恒说明生成物中不会有碳元素,则不可能生成碳酸钠,
利用盐酸来确定是否有碳酸钠生成,该实验设计如下,
实验步骤为:取少量探究1反应后的溶液于试管中,加入稀盐酸,
实验现象为:无现象,
实验结论为:生成物中无碳酸钠,
故答案为:反应物中不含碳元素,根据质量守恒定律判断不可能生成碳酸钠;
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量探究1反应后 的溶液于试管中,加入稀盐酸 |
无现象 | 生成物中 无碳酸钠 |
该反应中的另一生成物因为NaOH,故答案为:碱;NaOH;
[作出结论]因该反应的反应物为Na2O2和水,生成物为NaOH和O2,则该反应为2Na2O2+2H2O═4NaOH+O2↑,故答案为:2Na2O2+2H2O═4NaOH+O2↑.
点评:本题以脱脂棉滴水燃烧魔术为信息来探究过氧化钠与水反应的产物,学生应熟悉物质的性质及元素守恒、溶液的性质等来解答,较好的考查了学生综合应用知识来解决问题的能力、实验探究的能力、归纳整合的能力.

练习册系列答案
相关题目