题目内容
【题目】在一定质量的氯酸钾中加入少量的二氧化锰并加热到不再产生气体为止,下图中能正确表示反应前后各物质的质量变化(m)与时间(t)关系的是( )
A.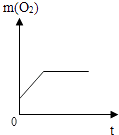
B.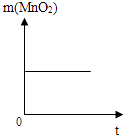
C.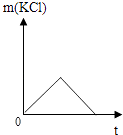
D.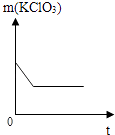
【答案】B
【解析】解:A、图示中,反应未开始即t=0时,即产生了氧气,与反应事实不符,故A不正确;
B、二氧化锰为反应的催化剂,在反应前后质量不变,故B正确;
C、图示中,氯化钾先随反应时间而增大,后又随反应时间而减小,与反应事实不符,故C不正确;
D、图示中,加热一开始氯酸钾就分解而减少,待反应一定时间后其质量稳定在一定量而不再改变,与完全反应的事实不相符合,故D不正确.
故选B.
【考点精析】通过灵活运用催化剂的特点与催化作用,掌握催化剂(触媒):在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质.(一变两不变)催化剂在化学反应中所起的作用叫催化作用即可以解答此题.

 阅读快车系列答案
阅读快车系列答案【题目】将一定量的丙烷(C3H8)和氧气置于一个密封容器中引燃,测得反应前后各物质的质量如表所示:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量(g) | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量(g) | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是( )
A.X可能是该反应的催化剂
B.X可能含有氢元素
C.X只含碳元素
D.X是纯净物
【题目】将一定量的丙烷(C3H8)和氧气置于一个密封容器中引燃,测得反应前后各物质的质量如表所示:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量(g) | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量(g) | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是( )
A.X可能是该反应的催化剂
B.X可能含有氢元素
C.X只含碳元素
D.X是纯净物
【题目】在高温下,铁与水蒸气能发生反应生成一种常见铁的氧化物和一种气体,某学习小组的同学对此反应很感兴趣,在小组集体协作下设计了如图实验,以探究铁粉与水蒸气反应后的产物,也邀请你一起来完成下列探究: 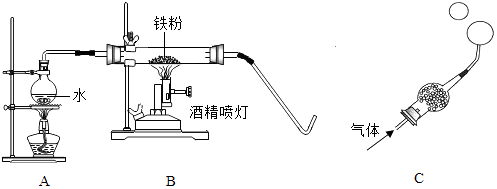
【猜想与假设】猜想一:生成的气体可能是氢气;猜想二:生成的气体可能是氧气.
【实验探究】将生成的气体通入C装置.球形管里装有碱石灰干燥剂.导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡.当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
(1)【推断】生成的气体是 .
(2)探究试管中剩余固体成分是什么? 【查阅资料】
Ⅰ.铁的氧化物①只有是Fe2O3红棕色,其余FeO、Fe3O4均为黑色;
②只有Fe3O4能被磁铁吸引.
Ⅱ.铁的氧化物都能与盐酸反应,但没有气体生成.
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是 .
(3)【实验探究】
实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量 | 无气泡产生,黑色固体是 |
(4)【实验结论】铁与水蒸气反应的化学方程式为: .
(5)【拓展延伸】Ⅰ.铁、镁混合物5.6g与足量稀硫酸反应,生成的氢气质量不可能是( )
A.0.2g
B.0.3g
C.0.4g
D.0.5g
(6)Ⅱ.某同学为探究铁合金中铁的质量分数,先后进行了四次实验(铁合金中除铁外,其余成分不与稀硫酸反应),实验数据如表.根据该同学的实验,试回答以下问题:
第一次 | 第二次 | 第三次 | 第四次 | |
所取合金的质量∕g | 10 | 10 | 20 | 30 |
所加稀硫酸的质量∕g | 100 | 120 | 80 | X |
生成氢气的质量∕g | 0.2 | 0.2 | 0.2 | Y |
表中第四次实验中,合金里的铁恰好与稀硫酸完全反应,则其中X=Y= .
(7)该铜铁合金中铁的质量分数是多少?(写出计算过程)
