题目内容
以下对 、
、 、
、 、
、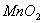 四种物质组成的说法中,正确的是( )
四种物质组成的说法中,正确的是( )
A. 都含有氧分子 B. 都含有2个氧原子
C. 都含有氧元素 D. 都含有2个氧元素
C

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
题目内容
以下对 、
、 、
、 、
、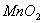 四种物质组成的说法中,正确的是( )
四种物质组成的说法中,正确的是( )
A. 都含有氧分子 B. 都含有2个氧原子
C. 都含有氧元素 D. 都含有2个氧元素
C

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案