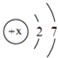题目内容
【题目】如图是元素周期表部分内容,请根据表中信息完成相关问题.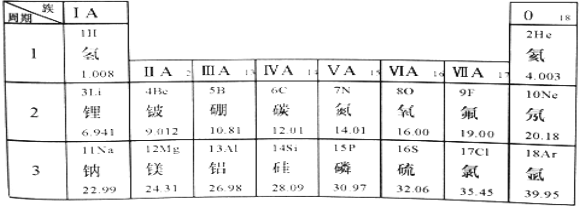
(1)铍原子的相对原子质量是 , 它属于(填“金属”或“非金属”)元素.
(2)不同种元素最本质的区别是 .
(3)原子序数为1、6、8的三种元素形成的常见化合物的化学式为 , 其中6号元素的化合价是 .
【答案】
(1)9.012;金属
(2)质子数不同
(3)H2CO3;+4
【解析】解:(1)由元素周期表中一个格的意义可知,铍原子的相对原子质量是9.012,它的名称中带有“钅”字旁,属于金属元素.(2)不同种元素最本质的区别是质子数不同,(3)原子序数为1、6、8的三种元素分别是氢、碳、氧元素,形成的常见化合物是碳酸,化学式为:H2CO3 , 由于氢显+1价,氧显﹣2价,由化合价原则可推出其中6号碳元素的化合价是+4.
故答为:(1)9.012,金属.(2)质子数不同,(3)H2CO3 , +4.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】图1是某兴趣小组在学习碱的性质时进行的探究活动,请要求回答问题.
(1)通过分析实验一可知,氢氧化钠会吸收空气中的 .
(2)实验二中观察到3个塑料瓶变瘪的程度为A>B>C,可证明CO2能与NaOH、Ca(OH)2反应,其中C瓶在实验中起作用.
(3)晓晓查阅资料了解到往Ba(OH)2溶液中滴加或通入下列图2中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀.
①写出D试管中反应的化学方程式 .
②不同的碱溶液中都含有OH﹣ , 所以,碱有一些相似的化学性质.上述关于Ba(OH)2性质的实验不能体现碱的相似性质的是(填字母序号)
(4)冬冬发现工业上使用的氢氧化钠固体标签如图3所示,于是对其所含杂质进行了探究.
【提出问题】
(5)【提出猜想】猜想I:查阅资料可知,工业用氢氧化钠可能含有NaCl.
猜想Ⅱ:工业用氢氧化钠可能含有Na2CO3 , 原因是(用简洁的文字表述).
(6)【进行实验】
实验步骤 | 实验现象 | 解释或结论 |
①取适量固体样品于试管中,加水溶解 | 固体全部溶解 | / |
②向①所得溶液中滴加过量的 | 一开始无明显变化,一会儿后产生能使澄清石灰水变浑浊的气体 | 样品中含有Na2C03 |
③向②所得溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有NaCl.反应的化学方程式为 |