题目内容
【题目】为了比较金属R与铁、铜的金属活动性强弱,某学校一个学习小组的同学进行了如下探究活动。
(查阅资料)铁的活动性比铜强。
(进行猜想)对三种金属的活动性顺序做出如下猜想
猜想一:R>Fe>Cu;猜想二:_____;猜想三:Fe>Cu>R
(收集证据)为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究
主要操作 | 主要现象 | 实验结论 | |
甲 | 将打磨好的铜丝插入盛有RSO4溶液的试管中 | _____ | 猜想一正确 |
乙 | 将打磨好的、粗细相同的R丝、铁丝分别插入体积和溶质的质量分数都相同的稀盐酸中 | R丝表面产生气泡速率比铁丝表面产生气泡速率_____(填“快”或“慢”) | |
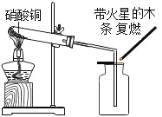
丙 | 将打磨好的、粗细相同的R丝、铁 丝分别在空气中灼烧 | R丝在空气中剧烈燃烧,铁丝在空气中只能发生_____现象,不能燃烧 |
铁丝在氧气中点燃可以发生剧烈燃烧,其化学方程式是_____。
(交流反思)三位同学交流讨论后认为,比较金属活动性强弱的方法有多种。
(归纳总结)他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与_____是否反应;
(2)金属与酸溶液是否反应或反应的剧烈程度;
(3)金属与氧气反应的难易和剧烈程度。
【答案】Fe>R>Cu 甲:无明显现象 乙:快 丙:红热  盐溶液
盐溶液
【解析】
[进行猜想]已知铁的活动性大于铜,则三种金属的活动性顺序有如下情况:R>Fe>Cu; Fe>R>Cu;Fe>Cu>R,故填Fe>R>Cu。
[收集证据]甲:猜想一正确,说明R的活动性比铜强,将打磨好的铜丝插入盛有RSO4溶液的试管中,铜不能置换RSO4中的金属R,观察到无明显现象,故填无明显现象;
乙:猜想一正确,说明R的活动性比铁强,将打磨好的、粗细相同的R丝、铁丝分别插入体积和溶质的质量分数都相同的稀盐酸中,观察到的现象是R丝表面产生气泡速率比铁丝表面产生气泡速率快,故填快;
丙:铁丝在空气中不能燃烧,只能发生红热现象,故填红热;
铁丝与氧气在点燃的条件下反应生成四氧化三铁,故反应的化学方程式写为:3Fe+2O2![]() Fe3O4。
Fe3O4。
[归纳总结](1)金属活动性强的金属能将金属活动性较弱的金属从其盐溶液中置换出来,所以可利用金属与盐溶液反应来比较金属活动性的强弱,故填盐溶液。