题目内容
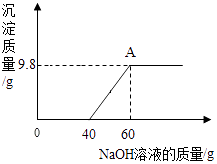
【题目】某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,实验测得相关数据如图所示: 
(1)反应生成氧气的质量为g.
(2)计算该过氧化氢溶液中溶质质量分数.
(3)实验表明硫酸铜溶液在该反应中也能起到二氧化锰的作用.若用5.6g无水硫酸铜代替二氧化锰进行本实验,计算剩余的溶液中溶质的质量分数.
【答案】
(1)1.6
(2)设过氧化氢的质量的质量为x,
2H2O2 |
| 2H2O+ | O2↑ |
68 | 32 | ||
x | 1.6g |
![]() ,
,
x=3.4g,
该过氧化氢溶液中溶质质量分数为: ![]() ×100%=5%,
×100%=5%,
答:该过氧化氢溶液中溶质质量分数为5%.
(3)剩余的溶液中硫酸铜的质量分数为: ![]() ×100%=7.8%,
×100%=7.8%,
答:剩余的溶液中硫酸铜的质量分数为7.8%.
【解析】解:(1)生成氧气的质量为:68.0g+1.0g﹣67.4g=1.6g,
【考点精析】本题主要考查了根据化学反应方程式的计算的相关知识点,需要掌握各物质间质量比=系数×相对分子质量之比才能正确解答此题.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目