题目内容
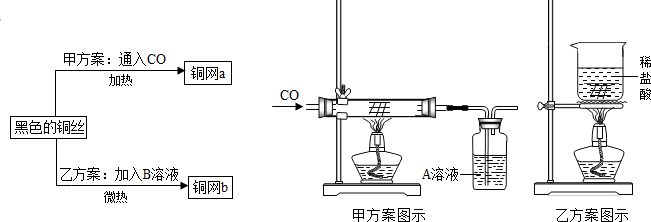
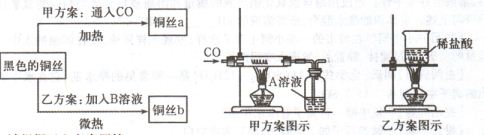
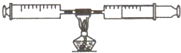
 课外活动小组对空气中氧气含量的测定做了如下实验:在由两个注射器组成的密闭系统内有50mL空气,如右图.然后给装有铜丝的玻璃管加热.同时交替推动两个注射器的活塞,至玻璃管内的铜丝变黑且较长时间内无进一步变化时停止.停止加热后,待冷却至室温将气体全部推至一个注射器内.
课外活动小组对空气中氧气含量的测定做了如下实验:在由两个注射器组成的密闭系统内有50mL空气,如右图.然后给装有铜丝的玻璃管加热.同时交替推动两个注射器的活塞,至玻璃管内的铜丝变黑且较长时间内无进一步变化时停止.停止加热后,待冷却至室温将气体全部推至一个注射器内.请根据你对上述实验的理解,回答下列问题
①验结束后,注射器内空气的体积减少了约
10
10
mL,这是因为空气中的氧气与铜反应,被消耗掉了
空气中的氧气与铜反应,被消耗掉了
.②在实验的加热过程中,交替缓慢推动两个注射器的目的是
使空气中的氧气充分与铜发生反应
使空气中的氧气充分与铜发生反应
.
.
.③上述实验只是粗略测定空气中氧气含量的一种方法,你认为造成该实验不够精确的可能原因是
铜丝未能完全反应掉空气中的氧气
铜丝未能完全反应掉空气中的氧气
.分析:①铜丝与空气中的氧充分反应,消耗掉空气中氧气,由空气中氧气的体积比容易求出空气减少的体积.
②由实验条件可推出交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应.
③交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应,但是推动的缓慢程度不易控制,易得出实验不精确的地方.
②由实验条件可推出交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应.
③交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应,但是推动的缓慢程度不易控制,易得出实验不精确的地方.
解答:解:①由于铜的氧化反应只消耗掉了空气中的氧气,而氧气在空气中约占空气体积的
,可得出答案:50mL×
=10ml;
②交替缓慢推动两个注射器的目的是使封闭空间的氧气与铜网充分接触,使空气中的氧气与铜网充分反应;
③交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应,但是推动的缓慢程度不易控制,易得出实验不精确的地方可能是因为空气中的氧气没有完全被铜网消耗掉.
故答案为:①10ml;空气中的氧气与铜反应,被消耗掉了;
②使空气中的氧气充分与铜发生反应;
③铜丝未能完全反应掉空气中的氧气.
| 1 |
| 5 |
| 1 |
| 5 |
②交替缓慢推动两个注射器的目的是使封闭空间的氧气与铜网充分接触,使空气中的氧气与铜网充分反应;
③交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应,但是推动的缓慢程度不易控制,易得出实验不精确的地方可能是因为空气中的氧气没有完全被铜网消耗掉.
故答案为:①10ml;空气中的氧气与铜反应,被消耗掉了;
②使空气中的氧气充分与铜发生反应;
③铜丝未能完全反应掉空气中的氧气.
点评:本题能通过实验探究的方式考查了铜与氧气的反应,空气中氧的体积分数,提高了学生学以致用的意识.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
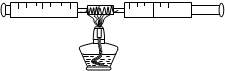 (1)课外活动小组对空气中氧气含量的测定做了如下实验:在由两个注射器组成的密闭系统内有50mL空气,如图.然后给装有铜丝的玻璃管加热.同时交替推动两个注射器活塞,至玻璃管内铜丝变黑且较长时间内无进一步变化时停止.停止加热后,待冷却至室温将气体全部推至一个注射器内.
(1)课外活动小组对空气中氧气含量的测定做了如下实验:在由两个注射器组成的密闭系统内有50mL空气,如图.然后给装有铜丝的玻璃管加热.同时交替推动两个注射器活塞,至玻璃管内铜丝变黑且较长时间内无进一步变化时停止.停止加热后,待冷却至室温将气体全部推至一个注射器内.