题目内容
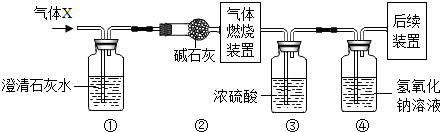
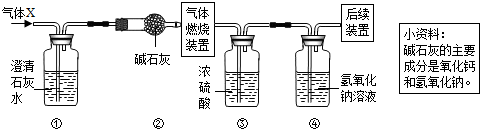
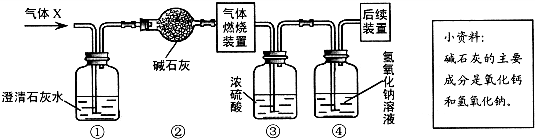
某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种.为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g.下列关于气体X成分的分析中,错误的是( )
A.一定没有二氧化碳
B.可能含有甲烷和氢气
C.可能只有甲烷
D.可能含有氢气和一氧化碳
【答案】分析:根据各装置的作用进行分析,①装置可以检验是否含有二氧化碳,碱石灰能吸收水分和酸性气体,浓硫酸是用来吸收水分的,氢氧化钠溶液用来吸收二氧化碳.装置①中无明显变化,排除了CO2;装置③增重1.8 g,说明生成了1.8g水;装置④增重2.2 g,说明生成了2.2g二氧化碳;根据水和二氧化碳的质量可计算出碳、氢元素的质量比,进而可以确定气体X的组成.
解答:解:A、气体X通过澄清石灰水时无明显变化,说明一定不含二氧化碳,分析正确;
B、该气体燃烧后生成水和二氧化碳,装置③增重1.8 g,说明生成了1.8g水,1.8g水中氢元素的质量为:1.8g× ×100%=0.2g;装置④增重2.2 g,说明生成了2.2g二氧化碳,碳元素的质量为2.2g×
×100%=0.2g;装置④增重2.2 g,说明生成了2.2g二氧化碳,碳元素的质量为2.2g× ×100%=0.6g,气体X中C:H=0.6g:0.2g=3:1;CH4中C:H=12:4=3:1;故X的组成可能是①只有甲烷,②可能含有氢气和一氧化碳,③可能同时含有甲烷、氢气和一氧化碳.通过以上分析,此项错误,符合题意;
×100%=0.6g,气体X中C:H=0.6g:0.2g=3:1;CH4中C:H=12:4=3:1;故X的组成可能是①只有甲烷,②可能含有氢气和一氧化碳,③可能同时含有甲烷、氢气和一氧化碳.通过以上分析,此项错误,符合题意;
C、通过以上分析,此项分析正确,不合题意;
D、通过以上分析,此项分析正确,不合题意.
故选B
点评:气体燃烧产生了水蒸气和二氧化碳,说明该气体中既含有氢元素,也含有碳元素.但我们在确定气体的组成时,还要根据碳氢的质量比来确定混合气体的组成.
解答:解:A、气体X通过澄清石灰水时无明显变化,说明一定不含二氧化碳,分析正确;
B、该气体燃烧后生成水和二氧化碳,装置③增重1.8 g,说明生成了1.8g水,1.8g水中氢元素的质量为:1.8g×
 ×100%=0.2g;装置④增重2.2 g,说明生成了2.2g二氧化碳,碳元素的质量为2.2g×
×100%=0.2g;装置④增重2.2 g,说明生成了2.2g二氧化碳,碳元素的质量为2.2g× ×100%=0.6g,气体X中C:H=0.6g:0.2g=3:1;CH4中C:H=12:4=3:1;故X的组成可能是①只有甲烷,②可能含有氢气和一氧化碳,③可能同时含有甲烷、氢气和一氧化碳.通过以上分析,此项错误,符合题意;
×100%=0.6g,气体X中C:H=0.6g:0.2g=3:1;CH4中C:H=12:4=3:1;故X的组成可能是①只有甲烷,②可能含有氢气和一氧化碳,③可能同时含有甲烷、氢气和一氧化碳.通过以上分析,此项错误,符合题意;C、通过以上分析,此项分析正确,不合题意;
D、通过以上分析,此项分析正确,不合题意.
故选B
点评:气体燃烧产生了水蒸气和二氧化碳,说明该气体中既含有氢元素,也含有碳元素.但我们在确定气体的组成时,还要根据碳氢的质量比来确定混合气体的组成.

练习册系列答案
相关题目
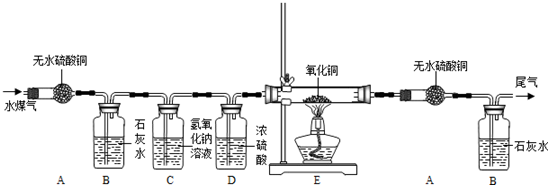

 H2、CO、和CH4都是初中化学常见的气体.
H2、CO、和CH4都是初中化学常见的气体.