题目内容
【题目】铝箔是现代生活中常见的包装材料。
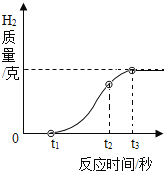
(1)用放置很久的铝箔与稀盐酸反应,产生氢气质量和反应时间关系如图所示。在0~t1时间段内,铝箔表面看不到明显气泡,原因是_______;在t2~t3时间段产生气泡的速度逐渐放缓,直到反应停止时,铝箔还有大量剩余。t2~t3时间段产生气泡速度放缓的原因_________。
(2)为进一步测量铝箔中单质铝的质量分数,现取1.9克铝箔样品与50.0克稀盐酸充分反应,铝箔完全溶解后剩余溶液的总质量为51.7克.计算样品中单质铝的质量分数。
【答案】(1)铝在空气中被氧气氧化,生成一层致密的氧化铝保护膜,阻止铝与稀盐酸反应;稀盐酸的溶质质量分数在反应中逐渐降低;
(2)94.7%
【解析】
(1)在0~t1时间段内,铝箔表面看不到明显的气泡,原因是:铝在空气中被氧气氧化,生成-层致密的氧化铝保护膜,阻止铝与稀盐酸反应;t2~t3时间段产生气泡速度放缓的原因是稀盐酸的溶质质量分数在反应中逐渐降低。
(2)生成氢气的质量:![]()
设生成0.2g氢气,需要参加反应的单质铝的质量为x

单质铝的质量分数:![]()

【题目】稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物(Y2O3)广泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含Y2O3约70%,含Fe2O3、CuO、SiO2等约30%)生产大颗粒氧化钇的一种工艺如下:
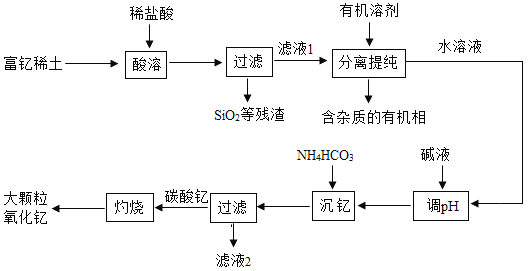
(1)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是______。
(2)“分离提纯”是为了除去滤液1中的_______(填化学式)。
(3)碳酸钇灼烧分解的化学方程式是______。
(4)为了获得大颗粒氧化钇,某小组研究了条件对产品直径的影响,相关数据如表(D50表示颗粒直径):
实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
沉淀反应温度/℃ | 60 | 80 | 85 | 93 | 93 | 93 |
料液浓度/(kgL) | 30 | 30 | 30 | 30 | 40 | 40 |
灼烧温度/℃ | 1100 | 1100 | 1100 | 1100 | 1100 | 1100 |
氧化钇D50/μm | 6.00 | 21.65 | 35.99 | 38.56 | 35.99 | 61.34 |
分析表中数据,其他条件不变时,若将灼烧温度均升高至1400℃ ,预期所得氧化钇D50最大的是___(填实验编号)。